
| 8.96L |
| 22.4L/mol |
| 3.01×1022 |
| 6.02×1023 |
| 10.2g |
| 34g/mol |
| m |
| n |
| 10g |
| 20g/mol |
| 8.96L |
| 22.4L/mol |
| 3.01×1022 |
| 6.02×1023 |
| 10.2g |
| 34g/mol |
| m |
| n |
| 26.7g |
| 0.2mol |
| 10g |
| 20g/mol |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、x+y>z |
| B、平衡向逆反应方向移动 |
| C、B的转化率降低 |
| D、C的体积分数升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝粉与硫酸铜溶液的反应 |
| B、氧气与一氧化碳的反应 |
| C、氢气还原氧化铜的反应 |
| D、氢氧化铁与稀硫酸的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
48 22 |
50 22 |
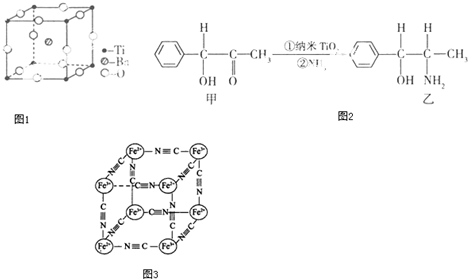
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等于20% | B、小于20% |
| C、大于20% | D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸镁溶于醋酸:CO32-+2CH3COOH=CO2↑+H2O+2CH3COO- |
| B、硫酸铜溶液中滴加氢氧化钡溶液:Ba2++SO42-═BaSO4↓ |
| C、碳酸氢钠溶液跟盐酸溶液反应:CO32-+2H+=CO2↑+H2O |
| D、氯化镁溶液中滴加澄清石灰水:Mg2++2OH-═Mg(OH)2↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com