
【题目】常温下,下列说法正确的是
A. 0.1mol/LNaHCO3溶液中:c(H+)+c(H2CO3)=c(CO32-)+c(OH-)
B. 0.1mol/LHCN和0.1mol/LNaCN的等体积混合溶液中:c(HCN)>c(Na+)>c(CN-)>c(H+)>c(OH-)
C. 0.1mol/LNa2C2O4溶液滴加HCl溶液至c(H2C2O4)=c(HC2O4-):3c(H2C2O4)>c(OH-)+c(Cl-)
D. 0.1mol/LNH4HSO4溶液滴加NaOH溶液至pH=7:c(Na+)=c(NH4+)+2c(NH3·H2O)>c(SO42-)
【答案】AD
【解析】A. 根据电荷守恒,c(H+)+ c(Na+)=2c(CO32-)+ c(HCO3-)+c(OH-),根据物料守恒,c(Na+)= c(H2CO3)+c(CO32-)+ c(HCO3-),将上述2式处理得c(H+)+c(H2CO3)=c(CO32-)+c(OH-),故A正确;B. 0.1mol/LHCN和0.1mol/LNaCN的等体积混合溶液显酸性,可以忽略NaCN的水解,主要考虑HCN的电离,则c(CN-)> c(Na+) >c(HCN) > c(H+)>c(OH-),故B错误;C. 假设0.1mol/LNa2C2O4溶液中含有0.1mol Na2C2O4,0.1mol/LNa2C2O4溶液滴加HCl溶液至c(H2C2O4)=c(HC2O4-),溶液中含有0.05molH2C2O4和0.05molNaHC2O4以及0.15molNaCl,溶液显酸性,以H2C2O4电离为主,则3c(H2C2O4)<c(Cl-)<c(OH-)+c(Cl-),故C错误;D. 假设0.1mol/LNH4HSO4溶液中含有1mol NH4HSO4,滴加NaOH溶液恰好生成0.5mol硫酸钠和0.5mol硫酸铵时,因为硫酸铵水解,溶液显酸性,此时c(Na+) =c(SO42-),要使得溶液pH=7,需要继续加入amol氢氧化钠反应生成![]() mol硫酸钠和amolNH3·H2O,因此c(Na+) >c(SO42-),n(Na+)=(1+a)mol,n(NH4+)+2 n(NH3·H2O)= (1-a+2a)mol=(1+a)mol,因此c(Na+)=c(NH4+)+2c(NH3·H2O) >c(SO42-),故D正确;故选D。
mol硫酸钠和amolNH3·H2O,因此c(Na+) >c(SO42-),n(Na+)=(1+a)mol,n(NH4+)+2 n(NH3·H2O)= (1-a+2a)mol=(1+a)mol,因此c(Na+)=c(NH4+)+2c(NH3·H2O) >c(SO42-),故D正确;故选D。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. N、O、F最高正价依次升高
B. 锂、钠、钾、铷单质与水反应置换出氢气越来越难
C. F2、Cl2、Br2、I2单质的熔点逐渐降低
D. Al3+、Na+、O2-微粒半径依次增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】经一定时间后,可逆反应aA+bBcC中物质的含量A%和C%随温度的变化曲线如图所示.下列说法正确的是( ) 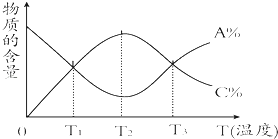
A.该反应在T1、T3温度时达到化学平衡
B.该反应在T2温度时达到化学平衡
C.该反应的逆反应是放热反应
D.升高温度,平衡会向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组用碱式碳酸铜[CuCO3·Cu(OH)2]制取铜粉并测定铜粉纯度的实验如下:
步骤1:将一定量的碱式碳酸铜置于烧杯中,向烧杯中加入N2H4的水溶液,边搅拌边加热,有大量的气体生成和红色铜析出,将沉淀过滤、低温干燥得红色粉末。
步骤2:称取1.9600 g红色粉末于烧杯中,缓慢加入足量稀硫酸,边加热边通入氧气使粉末完全溶解。冷却,将溶液移入100 mL 容量瓶中,用水稀释至刻度。
书骤3:准确量取20.00mL的溶液,调节溶液呈弱酸性,向其中加入过量的KI.,充分反应后,以淀粉溶液作指示剂,用0.2000mol/LNa2S2O3标准溶液滴定,滴定终点时共消耗Na2S2O3标准溶液30.00 mL.过程中所发生的反应如下:Cu2++I-![]() CuI↓+I3-(未配平),I3-+S2O32-=S4O62-+I-(未配平)。
CuI↓+I3-(未配平),I3-+S2O32-=S4O62-+I-(未配平)。
(1)步骤1中所发生反应的化学方程式为_________________。
(2)步骤2 中所发生反应的离子方程式为_________________。
(3)步骤3 中加入过量KI的作用是_________________。
(4)若铜粉中杂质不参与步骤3 的反应,通过计算确定红色粉末中含铜质量分数(写出计算过程)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),当它们混合时,即产生大量氮气和水蒸气,并放出大量热。已知0.4 mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.65 kJ的热量。
①写出反应的热化学方程式: ________________________________,其中氧化剂是____________,若反应中当有1molN2生成时转移的电子物质的量是__________。
②此反应用于火箭推进,除释放大量热和产生气体外,还有一个很大的优点是___________。
(2)已知:2CO(g) + O2(g) = 2CO2(g) △H= -566 kJ/mol
Na2O2(s) + CO2(g) = Na2CO3(s) + ![]() O2(g) △H= -226 kJ/mol
O2(g) △H= -226 kJ/mol
请写出常温下,过氧化钠与一氧化碳反应生成碳酸钠的热化学方程式:____________________。
(3)中学化学实验中的中和热的测定所需的玻璃仪器除了大烧杯、小烧杯、量筒外还有:_____,在大小烧杯之间填满碎泡沫(或纸条)其作用是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以软锰矿粉(主要含MnO2,还含有少量的Fe2O3、Al2O3等杂质)为原料制取高纯MnO2的流程如下:

(1)酸浸时所发生主要反应的离子方程式为_____________。
(2)酸浸时加入一定体积的硫酸,硫酸浓度不能过小或过大。当硫酸浓度偏小时,酸浸时会有红褐色渣出现,原因是_______。硫酸浓度不能过大的原因是_____________。
(3)过滤Ⅱ所得滤渣为MnCO3,滤液中溶质的主要成分是_____。
(4)焙烧MnCO3的装置如下图所示:

①焙烧时所发生反应的化学方程式为__________。
②焙烧一定时间后需转动石英管,目的是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为C、H、0、N、P等元素构成化合物甲、乙、丁及结构丙的示意图,下列说法错误的是
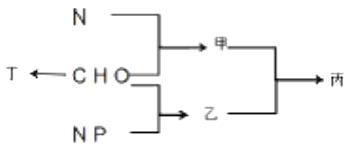
A. 若基因在结构丙上呈线性排列,则甲的单体用双缩脲试剂检测呈紫色
B. 若丁是真核细胞中良好的储能物质,则其合成场所为一种具膜的细胞器
C. 若丙是原核细胞内蛋白质合成场所,则乙彻底水解产物有6种
D. 若丙是一种生物膜,则其功能与膜上甲的种类和数量有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同浓度(c)、温度(T)条件下,蔗糖水解的瞬时速率(v)如下表。下列判断不正确的是
A. a=6.00 B. 同时改变反应温度和蔗糖的浓度,v可能不变
C. b<50 D. 50℃时,经过5s蔗糖浓度减少一半
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com