
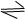 CH3COO-+H+,
CH3COO-+H+,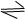 CH3COO-+H+;
CH3COO-+H+;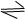 CH3COO-+H+,
CH3COO-+H+,

科目:高中化学 来源: 题型:
| A、将FeCl3饱和溶液煮沸可得到带正电荷的Fe(OH)3胶体 |
| B、0.5mol H2SO4与0.5mol Ba(OH)2完全反应所放出的热量即为中和热 |
| C、H2O的沸点高于H2S是因为O-H键的键能大于S-H键的键能 |
| D、向新制氯水中加入CaCO3可使溶液中HClO浓度增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 在某恒容的密闭容器中,可逆反应A(g)+B(g)?xC(g)有如图所示的关系曲线,下列说法正确的是( )
在某恒容的密闭容器中,可逆反应A(g)+B(g)?xC(g)有如图所示的关系曲线,下列说法正确的是( )| A、温度:T1>T2 |
| B、压强:p1>p2 |
| C、正反应是吸热反应 |
| D、x的值是2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,11.2L NO和11.2L O2混合后气体的分子总数为NA |
| B、标准状况下,2.24L Cl2通入足量H2O或NaOH溶液中转移的电子数均为0.1NA |
| C、0.1mol的白磷(P4)或四氯化碳(CCl4)中所含的共价键数均为0.4NA |
| D、在精炼铜或电镀铜的过程中,当阴极析出铜32g转移电子数均为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
 正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连(如图).下列有关说法正确的是( )
正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连(如图).下列有关说法正确的是( )| A、正硼酸晶体中只存在氢键 |
| B、H3BO3分子的稳定性与氢键无关 |
| C、分子中硼原子最外层为8e-稳定结构 |
| D、含1molH3BO3的晶体中有3mol氢键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com