
【题目】以柏林绿Fe[Fe(CN)6]为代表的新型可充电钠离子电池,其放电工作原理如图所示。下列说法正确的是

A. 放电时,Mo箔上的电势比Mg箔上的低
B. 充电时,Mo箔接电源的负极
C. 放电时,正极反应为Fe[Fe(CN)6]+2Na++2e-=Na2Fe[Fe(CN)6]
D. 充电时,外电路中通过0.2mol电子时,阴极质量增加3.55g
科目:高中化学 来源: 题型:
【题目】下列有关氧化还原反应的叙述正确的是( )
A.氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原
B.某金属元素M由化合态变为游离态,M一定被还原
C.用双线桥表示下列反应的电子转移
D.非金属单质在反应中只能作氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中正确的是( )
A. 氮原子的价电子排布图:![]()
B. 2p和3p轨道形状均为哑铃形,能量也相等
C. 价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素
D. 钠原子由1s22s22p63s1→1s22s22p63p1时,原子释放能量,由基态转化成激发态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. HClO、H2CO3、HNO3、HClO4的酸性依次增强
B. 苹果酸![]() 含有1个手性碳原子
含有1个手性碳原子
C. HCl、NH3、C2H5OH均易溶于水的原因之一是与H2O分子均形成氢键
D. 以极性键结合的分子不一定是极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 所含共价键数均为0.4NA的白磷(P4)和甲烷的物质的量相等
B. 1 mol Na与O2反应,生成Na2O和Na2O2的混合物共失去NA个电子
C. 1mol Na2O2固体中含有离子总数为4NA
D. 25℃时,pH=13的氢氧化钠溶液中约含有NA个氢氧根离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.熔融NaCl能导电,是因为通电时NaCl发生了电离
B.NaCl固体不导电,因为NaCl固体中无带电微粒
C.NH4NO3电离时产生了NH![]() 、NO
、NO![]() ,无金属离子,所以NH4NO3不是盐
,无金属离子,所以NH4NO3不是盐
D.NaHSO4在水溶液中电离生成了Na+、H+、SO![]() 三种离子
三种离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素的基态原子的核外电子有3种能量状态、5种空间状态,X是其中第一电离能最小的元素;元素Y的M层电子运动状态与X的价电子运动状态相同;元素Z位于第四周期,其基态原子的2价阳离子M层轨道全部排满电子。
(1)X基态原子的电子排布式为___________。
(2)X的氢化物(H2X)在乙醇中的溶解度大于H2Y,其原因是___________。
(3)在Y的氢化物(H2Y分子中,Y原子轨道的杂化类型是___________。
(4)Y与X可形成YX32-。
①YX32-的立体构型为___________(用文字描述)。
②写出一种与YX32-互为等电子体的分子的化学式___________。
(5)Z的氯化物与氨水反应可形成配合物[Z(NH3)4(H2O)2]Cl2,该配合物加热时,首先失去配离子中的配体是___________(写化学式)。
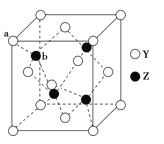
(6)Y与Z所形成化合物晶体的晶胞如图所示,该化合物的化学式为___________。其晶胞边长为540.0pm,密度为___________g·cm-3(列式并计算),a位置Y与b位置Z之间的距离为___________pm(列式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.100molL﹣1 NaOH溶液分别滴定20.00mL 0.100molL﹣1的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是( )
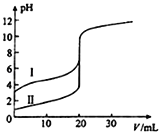
A. Ⅱ表示的是滴定醋酸的曲线
B. V(NaOH)=20.00mL时,两份溶液中c(Cl﹣)=c(CH3COO﹣)
C. pH=7时,滴定醋酸消耗的V(NaOH)小于20mL
D. V(NaOH)=10.00mL时,醋酸溶液中c(Na+)>c(CH3COO﹣)>c(H+)>c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一氧化二氯(Cl2O)是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸,42℃以上易分解。某化学兴趣小组设计如图装置以制备Cl2O(支撑及夹持装置已省略)。
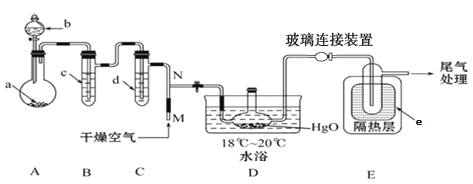
已知:① a中固体试剂是MnO2,b中试剂是浓盐酸。 ②Cl2O的部分性质如下表。
熔点 | 沸点 | 制备方法 |
-120.6 ℃ | 3.8℃ | 2HgO+2Cl2 = Cl2O+HgCl2·HgO |
请回答:
(1)指出该制备装置中存在的一个明显错误______________(经改进后进行有关实验)。
(2)装置C中盛有的试剂是______________。
(3)写出装置A中制备Cl2的化学方程式__________。
(4)装置D中采用18℃~20℃水浴的原因之一是如温度过低,反应速率慢,另一个可能的原因是 ___________。
(5)装置D、E间的连接方式与A、B、C间的连接方式有明显的差别,装置D、E间采用这种连接方式的理由是____________。
(6)Cl2O是市场上一种比较理想的饮水消毒剂,ClO2和Cl2O在消毒时自身均被还原为Cl-,则ClO2消毒能力是等质量Cl2O的_________倍(结果保留两位小数)
(7)文献报道说,Cl2O的另一种制备方法是利用Cl2与足量的Na2CO3溶液反应来制得,写出该反应的化学方程式:_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com