
以铬酸钾(K2CrO4)为原料用电化学法制备K2Cr2O7的装置如图,下列说法正确的是
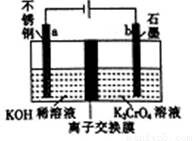
A. a极的电极反应为:2H2O+2e-=2OH-+H2↑
B. 电解过程中氢氧化钾溶液的浓度保持不变
C. b极上CrO42-发生氧化反应生成Cr2O72-
D. 电解过程中H+从右侧通过离子交换膜迁移到左侧
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源:2017届江西省新余市高三下学期第七次模拟考试理综化学试卷(解析版) 题型:填空题
(1)W原子的核外电子排布式为_________。
(2)均由X、Y、Z三种元素组成的三种常见物质A、B、C分别属于酸、碱、盐,其化学式依次为_________、__________、_________,推测盐中阴离子的空间构型为__________,其中心原子杂化方式为__________。
(3)Z、W两种元素电负性的大小关系为____;Y、Z两种元素第一电离能的大小关系为____。
(4)CO的结构可表示为C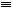 O,元素Y的单质Y2的结构也可表示为Y
O,元素Y的单质Y2的结构也可表示为Y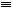 Y。右表是两者的键能数据(单位:kJ·mol-1):
Y。右表是两者的键能数据(单位:kJ·mol-1):
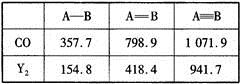
①结合数据说明CO比Y2活泼的原因:_____。
②意大利罗马大学Fulvio Cacace等人获得了极具研究意义的Y4分子,其结构如图所示,请结合上表数据分析,下列说法中,正确的是_____。
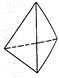
A.Y4为一种新型化合物 B.Y4与Y2互为同素异形体
C.Y4的沸点比P4(白磷)高 D.1 mol Y4气体转变为Y2将放出954.6kJ热量
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省株洲市高一下学期第一次月考化学试卷(解析版) 题型:填空题
X、Y、Z、M、R、Q为短周期主族元素,部分信息如下表所示:
X | Y | Z | M | R | Q | |
原子半径/nm | 0.037 | 0.077 | 0.074 | 0.071 | 0.102 | 0.099 |
主要化合价 | +1 | +4,-4 | -2 | -1 | +6,-2 | +7,-1 |
据此回答:
(1)下列试剂中,可用于检验YZ2和RZ2的混合物中含有RZ2的是_____________
澄清石灰水 B. 酸性高锰酸钾溶液
C. 品红溶液 D. 氢氧化钠溶液
(2)下列说法中,能作为R元素和Q元素非金属性强弱比较依据的是_____________
A.常温下,R的单质为固态,Q的单质为气态;
B.稳定性:X2R<XQ
C.酸性:X2R<XQ
(3)请写出Z元素的单质与Fe(OH)2悬浊液反应的化学方程式:_____________________。
(4)M元素的氢化物与SiO2反应的化学方程式:_______________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省株洲市高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列化学用语的书写正确的是
A. O2-的离子结构示意图: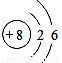
B. 质子数为27、中子数为60的Co原子: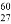 Co
Co
C. H2O的电子式:
D. 用电子式表示氢溴酸的形成过程为: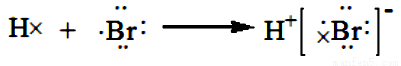
查看答案和解析>>
科目:高中化学 来源:2017届山东省菏泽市高三一模理综化学试卷(解析版) 题型:简答题
铬是由法国化学家沃克兰于1798年在巴黎发现的。目前铬被广泛应用于冶金、化工、铸铁、耐火及高精端科技等领域。
(1)铬元素基态原子的电子排布式为____________,其核外未成对电子数为__________。
(2)金属铬的第二电离能(ICr)和锰的第二电离能(IMn)分别为1590.6kJ·mol-1、1509.0 kJ·mol-1,ICr>IMn的原因是__________。
(3)雷氏盐(Reinecke salt)的化学式为NH4[Cr(NCS)4(NH3)2].H2O是一种易溶于水和乙醇的暗红色固体。
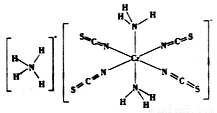
①雷氏盐中铬元素的化合价为_______,NH3与铬离子形成的化学键为__________。
②NCS-的立体构型是________,其中碳原子的杂化轨道类型为_______。SO2、CO2、BaCl2、SCl2四种分子中,与NCS-互为等电子体的是_____________。
③乙醇的沸点比溴乙烷高,其原因是__________。
(4)硒化铬的晶胞结构如图所示,晶胞参数为anm和bnm,则硒化铬的密度为____________g·cm-3(列出表达式即可)。

查看答案和解析>>
科目:高中化学 来源:2017届山东省菏泽市高三一模理综化学试卷(解析版) 题型:选择题
化学与生活、社会发展息息相关,下列说法正确的是
A. 洗涤剂除油污的原理与热碱液除油污的原理相同
B. 食品包装内放置生石灰与放置硅胶的作用相同
C. 聚乙烯和聚氯乙烯的单体相同
D. 自来水中加入漂白粉与加入硫酸铝的作用相同
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三第五次模拟考试理综化学试卷(解析版) 题型:选择题
2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户。用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示。下列说法正确的是
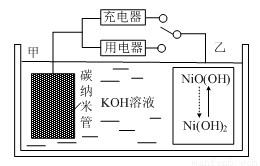
A.放电时,甲电极为正极,OH-移向乙电极
B.放电时,乙电极反应为:
NiO(OH)+H2O+e-=Ni(OH)2+OH-
C.充电时,电池的碳电极与直流电源的正极相连
D.电池总反应为H2+2NiOOH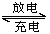 2Ni(OH)2
2Ni(OH)2
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省抚顺市高三3月模拟考试理科综合化学试卷(解析版) 题型:选择题
化学与科技、生产、生活等密切相关,下列说法正确的是
A. 中国的圆珠笔头一直需要进口笔尖钢,经过5年数不清的失败, 2016年9月,中国太钢集团利用家常和面原理在钢水中加入添加剂试验成功,造出圆珠笔头,可完全替代进口。由此信息可知笔尖钢为合金,且具有良好的切削性。
B. 日前从中国建筑材料科学研究总院获悉,天宫二号采用了该院研发改进的新材料,耐辐射石英玻璃,其主要成分为硅。
C. 用废轮胎、废电缆打碎制成的塑胶跑道,可以提高原子利用率
D. 塑化剂DEHP邻苯二甲酸二(2-乙基)己脂,对人体无害,可用作食品添加剂。
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江省大庆市高三第二次教学质量检测(二模)理科综合化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值,下列说法中正确的是
A. 某密闭容器中盛有0.2molSO2和0.1molO2,一定条件下充分反应,生成SO3分子数为0.2NA
B. 一定条件下,2.3gNa与O2完全反应生成3.6g产物时失去的电子书数0.1NA
C. 25℃时,0.1mol·L-1Na2S溶液中含有Na+的数目为0.2NA
D. 将1mL5.68mol·L-1的FeCl3饱和溶液制成胶体,可得到0.00568NA个Fe(OH)3胶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com