
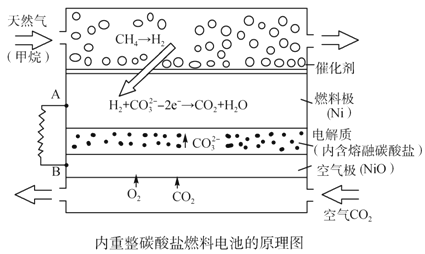
【题目】以熔融Li2CO3和K2CO3为电解质,天然气经重整催化作用提供反应气的燃料电池如右图。下列说法正确的是
A. 以此电池为电源电解精炼铜,当有0.1 mol e- 转移时,有3.2 g铜溶解
B. 若以甲烷为燃料气时负极电极反应式:CH4+5O2--8e-=CO32-+2H2O
C. 该电池使用过程中需补充Li2CO3和K2CO3
D. 空气极发生的电极反应式为O2+4e-+2CO2===2CO32-
【答案】D
【解析】试题分析:A、电解精炼铜,阳极上铜和比铜活泼的金属失电子变为金属阳离子进入电解质溶液,当有0.1 mol e-转移时,若只有铜放电,则有3.2 g铜溶解,粗铜有比铜更活泼的金属首先放电,所以溶解的铜小于3.2g,错误;B、根据图示信息,通入甲烷的电极是负极,在负极上,甲烷变为氢气,氢气发生失电子的氧化反应,即H2-2e-+CO32-==CO2+H2O,错误;C、该电池的电极反应为负极:H2-2e-+CO32-==CO2+H2O,正极:O2+4e-+2CO2==2CO32-,所以碳酸根离子的浓度不变,该电池使用过程中不需补充Li2CO3和K2CO3,错误;D、通入空气和CO2的混合气体一极为原电池的正极,发生还原反应,电极反应式为O2+4e-+2CO2==2CO32-,正确。


科目:高中化学 来源: 题型:
【题目】下列反应既不是水解反应,又不是氧化还原反应的是( )
A.Cl2+H2O![]() HCl+HClOB.H2S+H2O
HCl+HClOB.H2S+H2O![]() H3O++HS-
H3O++HS-
C.HCO![]() +H2O
+H2O![]() H2CO3+OH-D.NH
H2CO3+OH-D.NH![]() +H2O
+H2O![]() NH3·H2O+H+
NH3·H2O+H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色混合气体中可能含有![]() 、CO、
、CO、![]() 、
、![]() 气
气![]() 中的一种或几种,依次进行如下处理
中的一种或几种,依次进行如下处理![]() 假定每次处理均反应完全
假定每次处理均反应完全![]() :(1)通过碱石灰时,气体体积变小;(2)通过赤热的氧化铜时,固体变为红色;(3)通过无水硫酸铜粉末时,粉末变为蓝色;(4)通过澄清石灰水时,溶液变浑浊。由此可以确定原混合气体中
:(1)通过碱石灰时,气体体积变小;(2)通过赤热的氧化铜时,固体变为红色;(3)通过无水硫酸铜粉末时,粉末变为蓝色;(4)通过澄清石灰水时,溶液变浑浊。由此可以确定原混合气体中
A.一定含有![]() 、
、![]() ,可能含有
,可能含有![]() 、CO
、CO
B.一定含有![]() 、CO,可能含有
、CO,可能含有![]() 、
、![]()
C.一定含有CO、![]() ,可能含有
,可能含有![]() 、
、![]()
D.一定含有CO、![]() ,至少含有
,至少含有![]() 、
、![]() 的一种
的一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下述转化关系,回答问题:

已知:①+CH3Br![]() CH3+HBr;
CH3+HBr;
②C物质苯环上一卤代物只有两种。
(1)写出B物质的名称__________;D物质的结构简式________。
(2)写出反应②的类型________;反应⑤的条件________。
(3)写出反应⑥的化学方程式:________________________________。
(4)写出D+E反应的化学方程式:_______________。
(5)反应②还有可能生成一种C16H18的有机物,其苯环上一卤代物也只有两种,写出它的结构简式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图甲表示叶绿体的结构,图乙表示暗反应过程。请据图回答下列问题:

(l)叶绿体中的色素分布于图甲中的____ (填序号);四种色素能在滤纸条上分离,是因为____。
(2)叶绿体进行光合作用时,ATP的移动方向是从____到____(填序号),合成ATP所需的能量来自____。
(3)在光照强度、温度和CO2浓度三种环境因素中,能直接影响图乙所示过程的是 _________。若突然降低光照强度,则在短时间内叶绿体中C3和C5的含量变化分别是 _________、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2C2O4为二元弱酸。20℃时,配制一组c(H2C2O4)+ c(HC2O4-)+ c(C2O42-)="0.100" mol·L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如右图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是

A. pH=2.5的溶液中:c(H2C2O4)+ c(C2O42-)> c(HC2O4-)
B. c(Na+)="0.100" mol·L-1的溶液中:c(H+)+c(H2C2O4)=c(OH-)+ c(C2O42-)
C. c(HC2O4-)= c(C2O42-)的溶液中:c(Na+)>0.100 mol·L-1+ c(HC2O4-)
D. pH=7的溶液中:c(Na+)>2c(C2O42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:

已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O;②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下较安全;
③HClO2可看成是强酸。
(1)160 g·L-1NaOH溶液的物质的量浓度为__________________,若要计算该溶液溶质的质量分数,还需要的一个条件是____。
(2)在发生器中鼓入空气的作用可能是____(填序号)。
A.将SO2氧化成SO3,增强酸性
B.稀释ClO2以防止爆炸
C.将NaClO3氧化成ClO2
(3)吸收塔内的反应的化学方程式为____;
吸收塔的温度不能超过20℃,其目的是防止H2O2分解,写出H2O2分解的化学方程式:_________________。
(4)在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单的实验方法是___________。
(5)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中。除H2O2外,还可以选择的还原剂是__________________ (填序号)。
A.Na2O2 B.Na2S C.FeCl2 D.PbO(悬浊液)
(6)从滤液中得到NaClO2·3H2O粗晶体的实验操作依次是____(填序号)。
A.蒸馏 B.蒸发 C.灼烧 D.过滤 E.冷却结晶
要得到更纯的NaClO2·3H2O晶体必须进行的操作是____(填操作名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验:①0.1mol·L-1AgNO3溶液和0.1mol·L-1NaCl溶液等体积混合得到浊液a,过滤得到滤液b和白色沉淀c;② 向滤液b中滴加0.1mol·L-1KI溶液,出现浑浊;③ 向沉淀c中滴加0.1mol·L-1KI溶液,沉淀变为黄色。下列分析不正确的是
A.浊液a中存在沉淀溶解平衡:AgCl(s)![]() Ag+(aq)+ Cl-(aq)
Ag+(aq)+ Cl-(aq)
B.滤液b中不含有Ag+
C.③中颜色变化说明AgCl 转化为AgI
D.实验可以证明AgI比AgCI更难溶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.油脂皂化反应得到高级脂肪酸盐与甘油
B.在一定条件下,苯与液溴、硝酸、硫酸作用生成溴苯、硝基苯、苯磺酸的反应都属于取代反应
C.己烷有4种同分异构体,它们的熔点、沸点各不相同
D.聚合物(![]() )可由CH3CH=CH2和CH2=CH2加聚制得
)可由CH3CH=CH2和CH2=CH2加聚制得
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com