
【题目】能一次区分CH3COOH、CH3CH2OH、![]() 、
、![]() 四种物质的试纸或试剂是( )
四种物质的试纸或试剂是( )
A.H2OB.Na2CO3稀溶液
C.石蕊试液D.NaHSO4溶液
【答案】BC
【解析】
A. CH3COOH、CH3CH2OH与水均互溶,苯与硝基苯与水均互不相容,故A错误;
B. CH3COOH与Na2CO3溶液反应有气泡,CH3CH2OH与Na2CO3溶液互溶不分层,苯和硝基苯与Na2CO3溶液混合都分层,但苯在上层,硝基苯在下层,因此用Na2CO3溶液可以区别,故B正确;
C. CH3COOH与石蕊试液显红色,CH3CH2OH与石蕊试液互溶不分层,苯和硝基苯与石蕊试液混合都分层,但苯在上层,硝基苯在下层,因此用石蕊试液也可以区别,故C正确;
D. CH3COOH、CH3CH2OH与碳酸氢钠溶液均互溶,苯与硝基苯与碳酸氢钠溶液均互不相容,故D错误;
答案选BC。


科目:高中化学 来源: 题型:
【题目】关于如图微生物燃料电池结构示意图的说法:①微生物促进了电子的转移 ②微生物所在电极区放电时发生还原反应 ③放电过程中,H+从正极区移向负极区 ④正极反应式为:MnO2+4H++2e-===Mn2++2H2O正确的是( )

A. ④ B. ①③
C. ①④ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应2A(s)+3B(g) ![]() C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )
C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )
①增加A的量,平衡向正反应方向移动
②升高温度,平衡向逆反应方向移动,v(正)减小
③压强增大一倍,平衡不移动,v(正)、v(逆)不变
④增大B的浓度,v(正)>v(逆)
⑤加入催化剂,B的转化率提高
A.①②B.④C.③D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
(1)KIO3的化学名称是_______。
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:
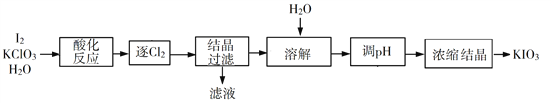
“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是________。“滤液”中的溶质主要是_______。“调pH”中发生反应的化学方程式为__________。
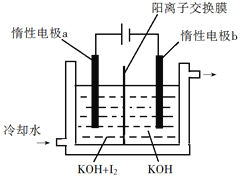
(3)KIO3也可采用“电解法”制备,装置如图所示。
①写出电解时阴极的电极反应式______。
②电解过程中通过阳离子交换膜的离子主要为_________,其迁移方向是_____________。
③与“电解法”相比,“KClO3氧化法”的主要不足之处有______________(写出一点)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的叙述正确的是( )
A.为确定![]() 是强酸还是弱酸,可测NaHA溶液的pH,若
是强酸还是弱酸,可测NaHA溶液的pH,若![]() ,则
,则![]() 是弱酸;若
是弱酸;若![]() ,则
,则![]() 是强酸
是强酸
B.![]() 时,在氨水体系中不断通入
时,在氨水体系中不断通入![]() ,随着
,随着![]() 的通入,
的通入,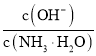 不断减少
不断减少
C.常温下。将等体积、等物质的量浓度的![]() 与NaC1溶液混合,析出部分
与NaC1溶液混合,析出部分![]() 晶体,过滤,所得滤液
晶体,过滤,所得滤液![]() ,则滤液中:
,则滤液中:![]()
![]()
D.室温下,将![]()
![]() 固体溶于水配成100mL溶液,向溶液中加入
固体溶于水配成100mL溶液,向溶液中加入![]() ,所得溶液中
,所得溶液中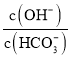 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA代表阿伏加德罗常数的数值,下列说法正确的是
A.常温常压下,3.4g NH3含N—H 键0.2 NA
B.标准状况下,1.4g N2、CO混合气体体积约为1.12 L
C.常温常压下,100 mL 0.1mol·L—1的过氧化氢水溶液中含氢原子的数目为0.02 NA
D.常温常压下,0.1 mol·L-1CH3COONa溶液中,c(CH3COO—)小于0.1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、磷、砷是原子序数依次增大的同一主族的三种元素,其化合物在工业农业中有重要用途。
(1)氮有多种重要的化合物。其中,N2O可用作发泡剂。
①NH3在加热和有催化剂的条件下,可以与O2反应生成N2O,该反应的化学方程式是_________。
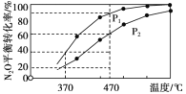
②在体积为1L的密闭容器中充入1mol N2O气体,发生反应2N2O(g) ![]() 2N2(g)+O2(g)。在不同温度下N2O的平衡转化率如下图所示。该反应的△H_________0(填“>”、“<”或“=” ),P1_______P2(填“大于”、“小于”或“等于”),370℃时,该反应的平衡常数K=_________。
2N2(g)+O2(g)。在不同温度下N2O的平衡转化率如下图所示。该反应的△H_________0(填“>”、“<”或“=” ),P1_______P2(填“大于”、“小于”或“等于”),370℃时,该反应的平衡常数K=_________。
(2)PH3和NH3与卤化氢的反应相似,产物的结构与性质也相似,下列对PH3与HCl反应产物的推断正确的是_________(选填字母序号)。
a.能与NaOH溶液反应 b.含有离子键与非极性共价键 c.水溶液显酸性
(3)三价砷有剧毒,五价砷毒性减弱。含As2O3的污水可被次氯酸钠碱性溶液转化为AsO43-而降低毒性。该反应的离子方程式是_________。
(4)HNO3、H3PO4、H3AsO4的酸性由强到弱的关系是________,请用原子结构理论解释原因__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,22.4L己烯中含有碳氢键数目为12NA
B.100g质量分数17%H2O2溶液中极性键数目为NA
C.65gZn与一定量的浓硫酸完全反应得混合气体的分子数为NA
D.电解精炼铜时阳极减轻32 g,电路中转移电子数目一定为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,将1.0L c mol·L-1 CH3COOH溶液与0.1mol NaOH固体混合,使之充分反应。然后向该混合溶液中通入HCl气体或加入NaOH固体(忽略体积和温度变化),溶液pH随通入(或加入)物质的物质的量的变化如图所示。下列叙述错误的是( )
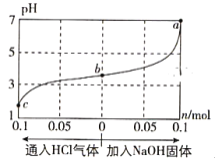
A. 水的电离程度:a>b>c
B. c点对应的混合溶液中:c(CH3COOH)>c(Na+)>c(OH-)
C. a点对应的混合溶液中:c(Na+)=c(CH3COO-)
D. 该温度下,CH3COOH的电离平衡常数![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com