
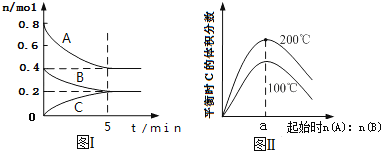
【题目】【2017孝义市模拟】在体积为2L的恒容密闭容器中发生反应xA(g)+yB(g)zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A)n(B)的变化关系.则下列结论正确的是( )
A.200℃时,反应从开始到平衡的平均速率v(B)=0.04molL﹣1min﹣1
B.图Ⅱ所知反应xA(g)+yB(g)zC(g)的△H<0,且a=2
C.若在图Ⅰ所示的平衡状态下,再向体系中充入He,重新达到平衡前v(正)>v(逆)
D.200℃时,向容器中充入2 mol A 和1 mol B,达到平衡时,A 的体积分数小于50%
【答案】D
【解析】A.由图Ⅰ可知,200℃时5min达到平衡,平衡时B的物质的量变化量为0.4mol﹣0.2mol=0.2mol,故v(B)= =0.02 molL﹣1min﹣1,故A错误;B.由图Ⅱ可知,n(A):n(B)一定时,温度越高平衡时C的体积分数越大,说明升高温度平衡向正反应移动,升高温度平衡向吸热反应移动,故正反应为吸热反应,即△H>0,图Ⅰ可知,200℃时平衡时,A的物质的量变化量为0.8mol﹣0.4mol=0.4mol,B的物质的量变化量为0.2mol,在一定的温度下只要A、B起始物质的量之比刚好等于平衡化学方程式化学计量数之比,平衡时生成物C的体积分数就最大,A、B的起始物质的量之比=0.4mol:0.2mol=2,故B错误;C.恒温恒容条件下,通入氦气反应混合物的浓度不变,平衡不移动,故v(正)=v(逆),故C错误;D.由图Ⅰ可知,200℃时平衡时,A、B、C的物质的量变化量分别为0.4mol、0.2mol、0.2mol,物质的量之比等于化学计量数之比,故x:y;z=0.4mol:0.2mol:0.2mol=2:1:1,平衡时A 的体积分数为
=0.02 molL﹣1min﹣1,故A错误;B.由图Ⅱ可知,n(A):n(B)一定时,温度越高平衡时C的体积分数越大,说明升高温度平衡向正反应移动,升高温度平衡向吸热反应移动,故正反应为吸热反应,即△H>0,图Ⅰ可知,200℃时平衡时,A的物质的量变化量为0.8mol﹣0.4mol=0.4mol,B的物质的量变化量为0.2mol,在一定的温度下只要A、B起始物质的量之比刚好等于平衡化学方程式化学计量数之比,平衡时生成物C的体积分数就最大,A、B的起始物质的量之比=0.4mol:0.2mol=2,故B错误;C.恒温恒容条件下,通入氦气反应混合物的浓度不变,平衡不移动,故v(正)=v(逆),故C错误;D.由图Ⅰ可知,200℃时平衡时,A、B、C的物质的量变化量分别为0.4mol、0.2mol、0.2mol,物质的量之比等于化学计量数之比,故x:y;z=0.4mol:0.2mol:0.2mol=2:1:1,平衡时A 的体积分数为![]() =0.5,200℃时,向容器中充入2 mol A 和1 mol B达到平衡等效为原平衡增大压强,平衡向正反应移动,A的增大,故达到平衡时,A 的体积分数小于0.5,故D正确;故选D。
=0.5,200℃时,向容器中充入2 mol A 和1 mol B达到平衡等效为原平衡增大压强,平衡向正反应移动,A的增大,故达到平衡时,A 的体积分数小于0.5,故D正确;故选D。


科目:高中化学 来源: 题型:
【题目】【2016盐城三模】实验室制取高纯NaI晶体(无色)可按下列步骤进行:按化学计量称取各原料,在三颈烧瓶中(如图)先加入适量的高纯水,然后按Na2CO3、I2和水合肼的投料顺序分批加入.
已知:①I2+Na2CO3═NaI+NaIO+CO2↑;△H<0
3I2+3Na2CO3═5NaI+NaIO3+3CO2↑;△H<0
②I2(s)+I﹣(aq)═I3﹣(aq);
③水合肼(N2H4H2O)具有强还原性,可分别将IO﹣、IO3﹣和I2还原为I﹣,本身被氧化为N2(放热反应);100℃左右水合肼分解为氮气和氨气等.
(1)常温常压时,I2与Na2CO3溶液反应很慢,下列措施能够加快反应速率的是 (填字母).
a.将碘块研成粉末 b.起始时加少量NaI
c.将溶液适当加热 d.加大高纯水的用量
(2)I2与Na2CO3溶液反应适宜温度为40~70℃,温度不宜超过70℃,除防止反应速率过快,另一个原因是 .
(3)加入稍过量水合肼发生反应的离子方程式为 (只写一个).
(4)整个实验过程中都需要开动搅拌器,其目的是 .
(5)反应的后期I2与Na2CO3溶液反应难以进行,此阶段需对投料顺序作适当改进,改进的方法是 .
(6)所得溶液(偏黄,且含少量SO42﹣,极少量的K+和Cl﹣)进行脱色、提纯并结晶,可制得高纯NaI晶体.实验方案为:在溶液中加入少量活性炭煮沸、
(实验中需使用的试剂有:HI溶液,Na2CO3溶液、Ba(OH)2溶液、高纯水及pH试纸;除常用仪器外须使用的仪器有:真空干燥箱)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2017宝山区二模】氮的单质及其化合物性质多样,用途广泛.
完成下列填空.
(1)科学家正在研究利用催化技术将超音速飞机尾气中的NO和CO转变成CO2和N2:2NO+2CO![]() 2CO2+N2+Q(Q>0)
2CO2+N2+Q(Q>0)
某温度下测得该反应在不同时间的CO浓度如表:
时间(s) 浓度(mol/L) | 0 | 1 | 2 | 3 | 4 | 5 |
c(CO) | 3.60×10﹣3 | 3.05×10﹣3 | 2.85×10﹣3 | 2.75×10﹣3 | 2.70×10﹣3 | 2.70×10﹣3 |
该反应平衡常数K的表达式为 ;温度升高,K值 (选填“增大”、“减小”、“不变”);前2s内的平均反应速率v(N2)= ;若上述反应在密闭容器中发生,达到平衡时能提高NO转化率的措施之一是 .
(2)工业合成氨的反应温度选择500℃左右的原因是 .
(3)实验室在固定容积的密闭容器中加入1mol氮气和3mol氢气模拟工业合成氨,反应在一定条件下已达到平衡的标志是 .
a.N2、H2、NH3的浓度之比为1:3:2
b.容器内的压强保持不变
c.N2、H2、NH3的浓度不再发生变化
d.反应停止,正、逆反应的速率都等于零
(4)常温下向含1mol溶质的稀盐酸中缓缓通入1mol NH3(溶液体积变化忽略不计),反应结束后溶液中离子浓度由大到小的顺序是 ;在通入NH3的过程中溶液的导电能力 (选填“变大”、“变小”、“几乎不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化不可能通过一步实验直接完成的是( )
A.Al(OH)3→Al2O3B.Al2O3→Al(OH)3C.Al→AlO2﹣D.Al3+→AlO2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列条件一定能使反应速率加大的是( )
①增加反应物的物质的量 ②升高温度 ③缩小反应容器的体积 ④不断分离出生成物
A.全部B.①②C.②D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016樟树市一模】在某温度下,将H2和I2各1mol的气态混合物充入1L的密闭容器中,发生反应:H2(g)+I2(g)2HI(g)△H<0;5min后达到平衡状态,测得c(H2)=0.9molL﹣1,则下列结论中,不能成立的是( )
A.平衡时H2、I2的转化率相等
B.从反应开始至平衡的过程中,v(HI)=0.04molL﹣1min﹣1
C.其他条件不变再向容器中充入少量H2,I2的转化率提高
D.若将容器温度提高,其平衡常数K一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有硫酸钠、硫酸铝、硫酸镁三种无色的溶液,可用一种试剂将它们区别开来,该试剂是( )
A. 蒸馏水 B. 盐酸 C. 氢氧化钠溶液 D. 硝酸银溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2017青山区模拟】某温度下,在体积不变的容器中进行反应:CO(g)+2H2(g)CH3OH(g)△H1=﹣90.7kJmol﹣1.已知反应的起始浓度分别为:c(CO)=1mol/L,c(H2)=2.4mol/L;5min后反应达平衡,此时CO的转化率为50%.则下列说法正确的是( )
A.该反应属于熵增放热反应,一定能自发进行
B.5 min内H2的平均反应速率为0.1 mol/(Lmin)
C.其它条件不变的情况下,加入催化剂可提高CO的转化率
D.若该温度下,反应物的起始浓度c(CO)=4 mol/L,c(H2)=a mol/L,达到平衡后,c(CH3OH)=2 mol/L,则a=5.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列氯代烃中不能由烯烃与氯化氢加成直接得到的有
A.氯代环已烷B.2,2-二甲基-1-氯丙烷
C.2-甲基-2-氯丙烷D.2,2,4,4-四甲基-3-氯戊烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com