
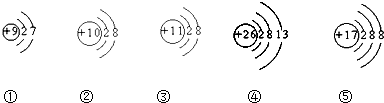
分析 根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子,据此进行分析解答.
解答 解:①质子数=9,核外电子数=9,质子数=核外电子数,为原子,
②质子数=10,核外电子数=10,质子数=核外电子数,为原子,
③质子数=9,核外电子数=10,质子数>核外电子数,失电子为阳离子,
④质子数=26,核外电子数=16,质子数>核外电子数,失电子为阳离子,
⑤质子数=17,核外电子数=18,质子数<核外电子数,得到电子为阴离子
故答案为:③④.
点评 本题考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键,题目难度不大.


 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:选择题
| A. | 将煤通过物理变化气化后再作为能源,可减少PM2.5引起的危害 | |
| B. | 普通玻璃属于无机非金属材料,有机玻璃属于新型无机非金属材料 | |
| C. | 在某爆炸事故救援现场,消防员发现存放金属钠、电石、甲苯二异氰酸酯等化学品的仓库起火,应立即用泡沫灭火器将火扑灭 | |
| D. | 硫酸亚铁片和维生素C同时服用,能增强治疗缺铁性贫血的效果 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.02mol/(L•s) | B. | 0.04mol/(L•s) | C. | 0.06mol/(L•s) | D. | 0.03mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 美国魏考克斯合成的一种有机分子,像一尊释迦牟尼佛.称为释迦牟尼分子.有关该有机分子的说法正确的是( )
美国魏考克斯合成的一种有机分子,像一尊释迦牟尼佛.称为释迦牟尼分子.有关该有机分子的说法正确的是( )| A. | 该有机物属于苯的同系物 | |
| B. | 1mol该有机物完全燃烧需消耗25molO2 | |
| C. | 1mol该有机物最多可以和10molH2发生加成反应 | |
| D. | 该有机物的一氯代产物的同分异构体有12种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,反应类型:加聚反应(或聚合反应)
,反应类型:加聚反应(或聚合反应) 反应类型:取代反应
反应类型:取代反应查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com