
���� ��1���ɢٿ�֪������������MnO4-����ԭΪMn2+���ɢڿ�֪������������MnO4-����ԭΪMnO2��
��2����PbO2Ͷ�뵽����MnSO4��Һ�н��裬��Һ��Ϊ�Ϻ�ɫ��˵��PbO2��Mn2+����ΪMnO4-��PbO2Ҳ���Խ�HCl����Ϊ������
��3����K2SO4��S�����ʵ���֮��Ϊ3��2���������ϵ���ֱ�Ϊ3��2�����ݵ���ת���غ����KMnO4��ϵ��������ԭ���غ�ȷ��K2S��KOH��K2MnO4��ϵ������Ԫ���غ��֪ȱ������ΪH2O��
�ڷ�Ӧ��ֻ��MnԪ�ػ��ϼ۽��ͣ����ݷ���ʽ����KMnO4�����ʵ������ٸ���MnԪ�ػ��ϼ۱仯����ת�Ƶ��ӣ�
��� �⣺��1���ɢٿ�֪������������MnO4-����ԭΪMn2+���ɢڿ�֪������������MnO4-����ԭΪMnO2������������ӱ���ԭ�IJ�������Һ��Ӱ�죬�ʴ�Ϊ������ԣ�
��2����PbO2Ͷ�뵽����MnSO4��Һ�н��裬��Һ��Ϊ�Ϻ�ɫ��˵��PbO2��Mn2+����ΪMnO4-������PbO2���������������������������������������ԣ�PbO2��KMnO4��PbO2Ҳ���Խ�HCl����Ϊ�����������������ữ��
��ѡ��B��
��3����K2SO4��S�����ʵ���֮��Ϊ3��2���������ϵ���ֱ�Ϊ3��2��ʧȥ�ĵ�������3��8+2��2=28�����ݵ���ת���غ�KMnO4��ϵ��Ϊ$\frac{28}{7-6}$=28������ԭ���غ㣬K2S��KOH��K2MnO4��ϵ���ֱ�Ϊ5��24��28����Ԫ���غ��֪ȱ������ΪH2O��ϵ��Ϊ12����ƽ��ʽΪ��28KMnO4+5K2S+24KOH=28K2MnO4+3K2SO4+3S��+12H2O��
�ʴ�Ϊ��28��5�� 24�� 28�� 3�� 2��12 H2O��
��������6.4g�����������ʵ���Ϊ$\frac{6.4g}{32g/mol}$=0.2mol����Ӧ��ֻ��MnԪ�ػ��ϼ۽��ͣ����ݷ���ʽ��֪KMnO4�����ʵ���Ϊ0.2mol��$\frac{28}{2}$=2.8mol����Ӧ��ת�Ƶ���Ϊ2.8mol����7-6��=2.8mol��
�ʴ�Ϊ��2.8��
���� ���⿼��������ԭ��Ӧ����������㡢��ƽ�������ԱȽϵȣ��Ѷ��еȣ����ջ�ѧ����ʽ������ƽ������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | b����ֱ����Դ�ĸ��� | |
| B�� | ʵ���������Һ�ĵ�������û�����Ա仯 | |
| C�� | ͨ��һ��ʱ��������������۲쵽����ɫ���� | |
| D�� | �����缫�����������ҵ缫����ͭ�������ʵ���������϶�ͭ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
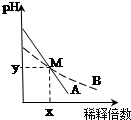
| A�� | ϡ��ǰ��c ��A����10 c ��B�� | |
| B�� | ϡ��ǰ��A��Һ��ˮ�������OH- Ũ����B��Һ����ˮ�������OH- Ũ�ȵ�10�� | |
| C�� | ��M�㣬A��B���ּ���Һ�������ӵ����ʵ���Ũ����� | |
| D�� | M��ʱA��B��Ũ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������Һ���ɰ�ɫ�������ټ�ϡ����������ܽ⣬����Һ��һ����Cl- | |
| B�� | ����ϡ���������ɫ��ζ���壬������ͨ�����ʯ��ˮ�У���Һ����ǣ�����Һ��һ����CO${\;}_{3}^{2-}$ | |
| C�� | �����Ȼ�����Һ�а�ɫ�����������ټ����ᣬ��������ʧ��һ����SO${\;}_{4}^{2-}$ | |
| D�� | ��������������Һ�����ɰ�ɫ�������ð�ɫ����Ѹ�ٱ�ɻ���ɫ�����ձ�ɺ��ɫ������Һ��һ������Fe3+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
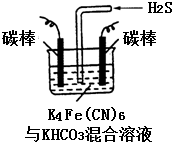 �����仯�������ճ�������Ӧ�ù㷺��
�����仯�������ճ�������Ӧ�ù㷺���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeCl3��NaHCO3�Ĺ����������ʱ�������������ˮ�ܽ�ʱ�г������ɣ� | |
| B�� | 25����60��ʱ��ˮ��pH��� | |
| C�� | �к͵�����������ʵ�����Ũ�ȵ�����ʹ��������ĵ�n��NaOH������� | |
| D�� | 2SO2��g��+O2��g���T2SO3��g���� 4SO2��g��+2O2��g��=4SO3��g���ġ�H��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Һ̬HCl����̬NaCl�������磬����HCl��NaCl�Ƿǵ���� | |
| B�� | NH3��CO2��Cl2��ˮ��Һ���ܵ��磬����NH3��CO2��Cl2���ǵ���� | |
| C�� | ǿ������ڹ�̬��Һ̬ʱ�����ܲ����� | |
| D�� | ͭ��ʯī�����磬���������ǵ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com