
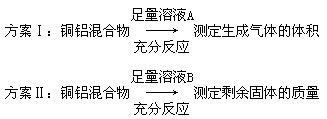
| A.溶液A和B均可以是盐酸或NaOH溶液 |
| B.溶液A和B均可以选用稀硝酸 |
| C.若溶液B选用浓硝酸,则测得铜的质量分数偏小 |
| D.实验室方案Ⅱ更便于实施 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.Al→Al2O3→NaAlO2→Al(OH)3 |
| B.Si→SiO2→H2SiO3→Na2SiO3 |
| C.N2→NO2→HNO3→NO |
D. |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
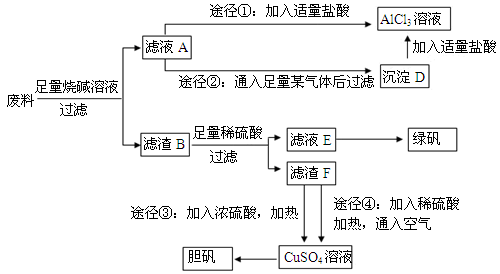
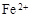 和
和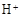 外,还可能存在 (用元素符号表示)。
外,还可能存在 (用元素符号表示)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaHCO3饱和溶液,又有CaCO3沉淀生成 |
| B.向Na2CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1∶2 |
| C.等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同 |
| D.向Na2CO3饱和溶液中通入CO2,有NaHCO3结晶析出 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na和O2 | B.NaOH和CO2 |
| C.Na2O2和CO2 | D.NaHCO3和Ca(OH)2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.生铁属于合金 |
| B.金属的冶炼过程通常是把金属阳离子氧化成单质的过程 |
| C.回收废旧金属既可以治理污染,又可以缓解资源短缺 |
| D.工业上电解氯化镁获得金属镁 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
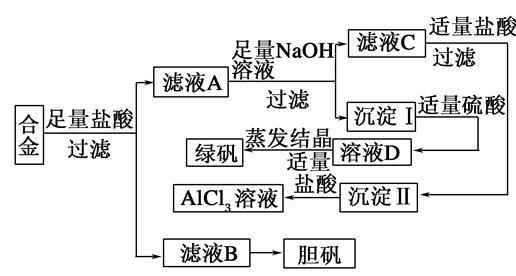
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
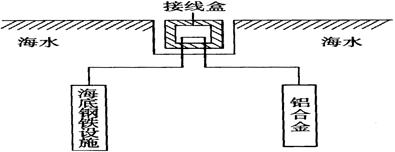
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com