
| A. | 1:3 | B. | 1:2 | C. | 2:3 | D. | 3:4 |
科目:高中化学 来源: 题型:选择题
| A. | 全氟丙烷(C3F8)与全氟甲烷(CF4)互为同系物 | |
| B. | 石墨能导电,所以石墨属于电解质 | |
| C. | 在化学反应中,原子的种类和数目均保持不变 | |
| D. | 干冰的气化、煤的气化均属于物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
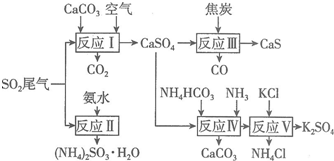
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中Na+数目增多 | |
| B. | 溶液中有氢气逸出 | |
| C. | 溶质的质量分数增大 | |
| D. | 溶液质量减少,溶质的质量分数不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

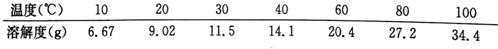
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 自然界中的氧气和二氧化碳通过光合作用与呼吸作用可以相互转化 | |
| B. | 实验室制氧气和二氧化碳都可通过分解反应制得 | |
| C. | 氧气和二氧化碳都可以用向上排空气法收集 | |
| D. | 一般情况下,氧气能支持燃烧,二氧化碳不能支持燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入20 g 固体NaOH,搅拌、溶解 | |
| B. | 将溶液加热浓缩至0.2 L | |
| C. | 加入10 mol/L的NaOH溶液0.1 L,再稀释至1.5 L | |
| D. | 加入1 L 1.5 mol/L的NaOH溶液混合均匀 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 A、B、C均是由短周期元素组成的单质,D、E、F、G、H、I均为化合物,F在常温常压下为液态,I为具有磁性的黑色晶体,它们有如图所示的转化关系:
A、B、C均是由短周期元素组成的单质,D、E、F、G、H、I均为化合物,F在常温常压下为液态,I为具有磁性的黑色晶体,它们有如图所示的转化关系:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
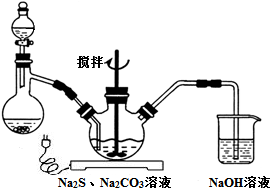
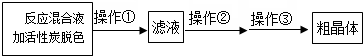
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com