
分析 (1)利用三段式分析:设A容器中反应中SO2转化的物质的量为2xmol,
A容器中 2SO2(g)+O2(g)?2SO3(g)
起始量(mol):2 1 0
变化量(mol):2x x 2x
平衡量(mol):2-2x 1-x 2 x
由题意可知,$\frac{3-x}{3}$=$\frac{0.8}{1}$,所以x=0.6,据此计算SO2的转化率;
(2)根据容器中的压强对化学平衡的影响;
(3)由于A、B的起始量成比例且与计量数之比相等,所以当A、B两容器连接后,打开开关使互通一段时间后又重新达到平衡时,压强与A容器的起始压强相同,所以连接后与连接前A容器的平衡状态为等效平衡,且起始量为A的3倍,据此计算;
(4)若开始时B中充入2mol SO2、1mol O2,则连通AB后与连通前的A为等效平衡,据此计算A容器的容积;
解答 解:(1)利用三段式分析:设A容器中反应中SO2转化的物质的量为2xmol,
A容器中 2SO2(g)+O2(g)?2SO3(g)
起始量(mol):2 1 0
变化量(mol):2x x 2x
平衡量(mol):2-2x 1-x 2x
由题意可知,$\frac{3-x}{3}$=$\frac{0.8}{1}$,所以x=0.6,则A中SO2的转化率为$\frac{0.6×2}{2}$×100%=60%,
故答案为:60%;
(2)根据反应可知2SO2(g)+O2(g)?2SO3(g),B容器充入SO2、O2的物质的量为A容器的2倍,所以平衡时A容器中的压强小于B容器,由于该反应是气体体积减小的反应,所以B中SO2的转化率大于A中的,
故答案为:<;
(3)由于A、B的起始量成比例且与计量数之比相等,所以当A、B两容器连接后,打开开关使互通一段时间后又重新达到平衡时,压强与A容器的起始压强相同,所以连接后与连接前A容器的平衡状态为等效平衡,且起始量为A的3倍,所以连接后A容器的体积为连接前的3倍,即为3×0.8L=2.4L,
故答案为:2.4;
(4)若开始时B中充入2mol SO2、1mol O2,则连通AB后与连通前的A为等效平衡,根据(3)中的计算方法可知,A容器的容积为2×0.8L=1.6L,
故答案为:1.6.
点评 本题考查化学平衡移动的判断,本题难度中等,注意等效平衡的理解和应用,掌握基础是解题关键.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲、乙中都是铝过量 | B. | 甲中铝不足、乙中铝过量 | ||
| C. | 甲中酸过量、乙中铝过量 | D. | 甲中酸过量、乙中铝过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
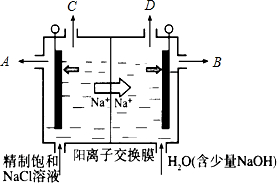 二氧化氯(ClO2)正逐步代替Cl2成为公认的高效、广谱、安全的水处理剂.当自来水厂用ClO2处理后水中含ClO2在0.1~0.8mg•L-1之间时,即达到合格标准.
二氧化氯(ClO2)正逐步代替Cl2成为公认的高效、广谱、安全的水处理剂.当自来水厂用ClO2处理后水中含ClO2在0.1~0.8mg•L-1之间时,即达到合格标准.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯水也是一种电解质 | |
| B. | 无论是酸性、中性还是碱性稀溶液,只要温度恒定,c(H+)×c(OH-)是一个常数 | |
| C. | 一定温度下,0.1mol•L-1的磷酸溶液中H+主要来自于酸的第一步电离 | |
| D. | 强碱溶液中不存在H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 被还原 | B. | 被氧化 | ||
| C. | 有可能被氧化,也有可能被还原 | D. | 由高价态变为零价 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在K2SO4与BaCl2两溶液反应时,增大压强 | |
| B. | 碱金属Cs与水反应时增大水的用量 | |
| C. | Fe与稀硫酸反应制取氢气时,改用浓硫酸 | |
| D. | Al与盐酸反应,加几滴氯化铜溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com