
| A. | 铝与氢氧化钠反应 | |
| B. | 向氯化铝溶液中加入过量氨水 | |
| C. | 含氟牙膏中加入氯化铝并不断充分搅拌 | |
| D. | 向硫酸铜溶液中通入过量氨气 |
分析 A.铝和过量氢氧根离子反应生成配合物;
B.氯化铝溶液中加入过量氨水只生成氢氧化铝沉淀;
C.氟离子和铝离子生成配合物;
D.向硫酸铜溶液中通入过量氨气,氨水多时生成四氨合铜离子,氨水少时生成氢氧化铜沉淀.
解答 解:A.铝和过量氢氧根离子反应生成Al(OH)4 -,所以能生成配合物,故A错误;
B.因为氢氧化铝只溶解于强酸强碱,所以氯化铝溶液中加入过量氨水只生成氢氧化铝沉淀,不会生成配合物,故B正确;
C.铝离子和氟离子反应生成配离子AlF6 3-,所以能生成配合物,故C错误;
D.向硫酸铜溶液中通入过量氨气,先产生蓝色氢氧化铜沉淀,继续滴加,形成配合物四氨合铜离子使沉淀溶解,离子方程式为Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+,后发生:Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++2OH-+4H2O,所以能生成配合物,故D错误;
故选B.
点评 本题考查了配合物的生成,明确物质的性质是解本题关键,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液中,NO3-、Na+、I-、Fe2+ | |
| B. | pH=13的溶液中,Cl-、Mg2+、CH3COO-、K+ | |
| C. | 水电离出的c(H+)=1×10-12mol•L-1溶液中,HCO3-、SO42-、Na+、NH4+ | |
| D. | pH=14的无色透明溶液中,K+、Na+、NO3-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
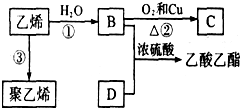 已知乙烯能发生如图转化:
已知乙烯能发生如图转化: ;反应类型:加聚反应.
;反应类型:加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
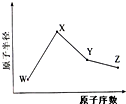 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
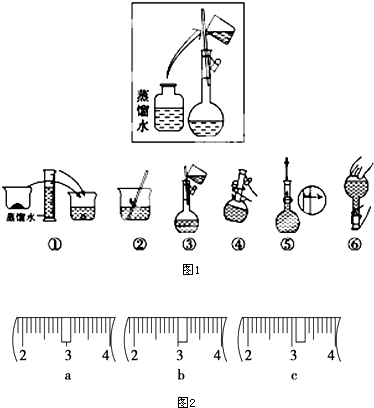 某同学帮助水质检测站配制230mL、1mol•L-1NaOH溶液以备使用.
某同学帮助水质检测站配制230mL、1mol•L-1NaOH溶液以备使用.| a | b | c | d | e | |
| 砝码大小/g | 100 | 50 | 20 | 10 | 5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com