
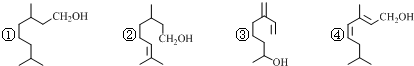
| A. | ①③④互为同分异构体 | |
| B. | ②③④互为同系物 | |
| C. | 上述四种物质中能使酸性KMnO4溶液褪色的只有②③④ | |
| D. | 上述物质分别与足量H2发生加成反应,共可得2种产物 |
分析 A.分子式相同、结构不同的有机物互称同分异构体;
B.结构相似,在分子组成上相差一个或n个-CH2原子团的有机物互称同系物;
C.碳碳双键和醛基、醇羟基位于边上的醇都能被酸性高锰酸钾溶液氧化;
D.分别与足量氢气发生加成反应后,①②④是同一种物质.
解答 解:A.分子式相同、结构不同的有机物互称同分异构体,③④同分异构体,故A错误;
B.结构相似,在分子组成上相差一个或n个-CH2原子团的有机物互称同系物,③④同分异构体,故B错误;
C.碳碳双键和醛基、醇羟基位于边上的醇都能被酸性高锰酸钾溶液氧化,这几种物质都能被酸性高锰酸钾溶液氧化,故C错误;
D.分别与足量氢气发生加成反应后,①②④是同一种物质,所以上述物质分别与足量H2发生加成反应,共可得2种产物,故D正确;
故选D.
点评 本题考查有机物结构和性质,为高频考点,侧重考查基本概念及官能团及其性质关系,明确官能团及其性质关系是解本题关键,题目难度不大.


 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:解答题
 用18mol/L的浓硫酸配制150.00mL 1.00mol/L硫酸:
用18mol/L的浓硫酸配制150.00mL 1.00mol/L硫酸:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1mol CO2、3mol H2 | a mol CO2、3a mol H2、 b mol CH3OH(g)、b mol H2O(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
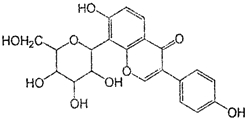
| A. | 该物质在一定条件下能发生消去反应、加成反应、取代反应 | |
| B. | 葛根素的分子式为C21H22O9 | |
| C. | 该物质在一定条件下能与碳酸氢钠溶液反应 | |
| D. | 一定条件下1 mol 该物质与H2反应最多能消耗7 mol H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
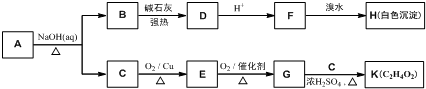

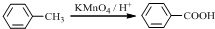
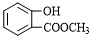 .
.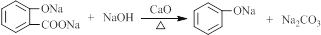 .
.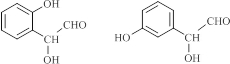 (写结构简式).
(写结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .固体甲溶于水后,溶液呈碱(酸、碱或中性),写出甲与水反应的化学方程式NH5+H2O=NH3•H2O+H2↑.
.固体甲溶于水后,溶液呈碱(酸、碱或中性),写出甲与水反应的化学方程式NH5+H2O=NH3•H2O+H2↑.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| C(NO)10-4 mol/L | 10.0 | 4.50 | C1 | 1.50 | 1.00 | 1.00 |
| C(CO)10-3 mol/L | 3.60 | 3.05 | C2 | 2.75 | 2.70 | 2.70 |
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | CO | H2 | |||
| i | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
| ii | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
| iii | 900 | a | b | c | d | t |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L空气中O2、N2分子数为NA | |
| B. | 0.1mol羟基中所含电子数目为NA | |
| C. | 钠与氧气反应时,每消耗4.6g钠时生成的阴离子数目为0.1NA | |
| D. | 25℃时,1.0L pH=13的Ba(OH)2溶液中含有的OH-数为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com