
【题目】按下图装置进行实验,并回答下列问题:
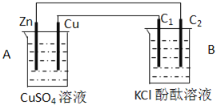
(1)判断装置的名称:A池为_________,B池为___________。
(2)铜极为______极,电极反应式为_________,石墨棒C1为___极,电极反应式为______________________,石墨棒C2附近发生的实验现象为___________________。
(3)当C2极析出224mL气体(标准状态时),锌的质量变化(增加或减少)_____g,CuSO4溶液的质量变化了(增加或减少了)______g。
【答案】 原电池 电解池 正极 Cu2++2e-=Cu 阳 2Cl--2e-=Cl2↑ 碳棒附近溶液变红且产生气体 减少0.65 增加0.01
【解析】
(1)锌能和硫酸铜发生置换反应,锌、铜和硫酸铜溶液构成原电池,因此A是原电池,则B是电解池。
(2)锌的金属性强于铜,则锌是负极,铜是正极,溶液中的铜离子得到电子,电极反应式是Cu2++2e-=Cu。石墨棒C1与电源的正极相连,为阳极,发生失去电子的氧化反应,即溶液中的氯离子放电,电极反应式为2Cl--2e-=Cl2↑;石墨棒C2和电源的负极相连,做阴极,溶液中的氢离子放电,同时破坏溶液中水的电离平衡,使阴极周围溶液显碱性,所以C2附近发生的实验现象为碳棒附近溶液变红且产生气体。
(3)224mL气体是氢气,物质的量是0.01mol,则转移0.02mol电子,所以根据电子的得失守恒可知消耗锌的物质的量是0.02mol÷2=0.01mol,质量是0.65g,即锌的质量减少0.65g。由于正极析出铜的质量是0.64g,所以溶液质量增加0.65g-0.64g=0.01g。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 3.0L0.1mol·L-1NaOH溶液中缓慢通入CO2至溶液增重8.8g时。溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
B. 常温下,将CH3COONa溶液和盐酸混合至溶液pH=7:c(Na+)>c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)=c(OH-)
C. 常温下,pH=6的NaHSO3溶液中:c(SO32-)- c(H2SO3)=9.9×10-7mol·L-1
D. Ksp (Fe(OH)3)=1.0×10-38,Ksp (Mg(OH)2)=1.0×10-11,则浓度均为0.1 mol·L-1氯化铁、氯化镁混合溶液,若除去溶液中的Fe3+,应将pH调至3~11。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置,通电后,发现Cu极附近溶液蓝色加深。下列说法正确的是( )
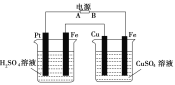
A. A极为负极,Cu为阳极
B. 左烧杯溶液和右烧杯溶液的pH都变小
C. 左烧杯溶液浓度变大,右烧杯溶液浓度不变
D. 左烧杯Pt极和右烧杯Fe极的电解产物物质的量之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对反应:aA(g)+bB(g)![]() cC(g)+dD(g) ΔH,反应特点与对应的图象的说法中不正确的是
cC(g)+dD(g) ΔH,反应特点与对应的图象的说法中不正确的是
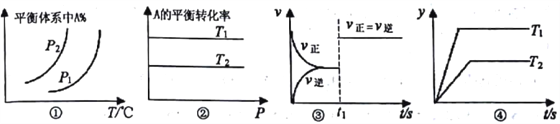
A. 图①中,若P1>P2,则该反应在较低温度下有利于自发进行
B. 图②中,若T2>T1,则△H<0 且a+b=c+d
C. 图③中t1时刻改变的条件一定是使用了催化剂
D. 图④中,若△H<0,则纵坐标不可能表示的是反应物的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.钠的摩尔质量等于它的相对原子质量
B.CH4的摩尔质量为16 g/mol
C.22.4 L任何气体的物质的量均为1 mol
D.1 mol 任何物质均含有NA个分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO2 与SO2能发生反应:NO2+SO2![]() SO3+NO,某研究小组对此进行相关实验探究。
SO3+NO,某研究小组对此进行相关实验探究。
(1)已知:2NO(g)+O2(g)![]() 2NO2(g) ΔH=-113.0kJmol-1
2NO2(g) ΔH=-113.0kJmol-1
2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6kJmol-1
2SO3(g) ΔH=-196.6kJmol-1
则NO2(g)+SO2(g)![]() SO3(g)+NO(g) ΔH=______________________。
SO3(g)+NO(g) ΔH=______________________。
(2)实验中,尾气可以用碱溶液吸收。NaOH 溶液吸收NO2时,发生的反应为:2NO2+2OH-=NO2-+NO3-+H2O,反应中的还原剂是__________;用NaOH 溶液吸收少量SO2的离子方程式为______________________________。
(3)在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n0(NO2)∶n0(SO2)]进行多组实验(各次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[a(NO2)]。部分实验结果如图所示:
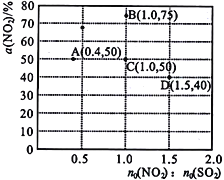
①当容器内_____(填标号)不再随时间的变化而改变时,可以判断反应达到了化学平衡状态。
a.气体的压强 b.气体的平均摩尔质量
c.气体的密度 d.NO2的体积分数
②如果要将图中C点的平衡状态改变为B点的平衡状态,应采取的措施是______________。
③若A 点对应实验中,SO2(g)的起始浓度为c0 molL-1,经过t min达到平衡状态,该时段化学反应速率v(NO2)=______________mol·L-1·min-1。
④图中C、D 两点对应的实验温度分别为Tc和Td,通过计算判断:Tc____Td(填 “>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤的烟气中含有SO2,为了治理雾霾天气,工厂采用多种方法实现烟气脱硫。
(1)“湿式吸收法”利用吸收剂与SO2发生反应从而脱硫。下列试剂中适合用作该法吸收剂的是______(填字母序号)。
a.石灰乳b.CaCl2溶液
(2)某工厂利用含SO2的烟气处理含Cr2O72-的酸性废水,吸收塔中反应后的铬元素以Cr3+形式存在,具体流程如下:
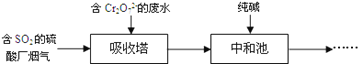
①用SO2处理含铬废水时,利用了SO2的______性。
②吸收塔中发生反应的离子方程式为____________________________________。
(3)该废水经处理后,测得有关数据如下(其他离子忽略不计):
离子 | Cr2O72- | Cr3+ | H + | Na + | SO42- |
浓度(mol/L) | a | 0.2×10-6 | 1.2×10-6 | 6.8×10-6 | 3.0×10-6 |
则a= ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列6种与人们生产生活相关的有机物:
① ![]() (日化用品香料) ②
(日化用品香料) ② ![]() (基础化工原料)
(基础化工原料)
③ ![]() (基础化工原料) ④
(基础化工原料) ④ 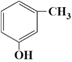 (生产农药的原料)
(生产农药的原料)
⑤ ![]() (食用香料) ⑥
(食用香料) ⑥ ![]() (食品防腐剂)
(食品防腐剂)
请回答:
(1)属于酯类的是______(填序号)。
(2)与②互为同系物的是______(填序号)。
(3)与①互为同分异构体的是______(填序号)。
(4)用系统命名法给②命名,其名称为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物完全燃烧只生成CO2和H2O,两者的物质的量之比为2∶3,因而可以说
A. 该有机物中含C、H、O三种原子
B. 该化合物是乙烷
C. 该化合物中C、H原子个数比为2:3
D. 该化合物中含C原子和H原子,但不能确定是否含有O原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com