
| A. | NH3极易溶于水,可用于工业制冷剂 | |
| B. | HNO3具有酸性,可用于制备硝酸盐原料 | |
| C. | NH4 NO3易溶于水,可用于制造高温材料 | |
| D. | N2难溶于水,可用于合成氨原料 |
分析 A.液氨汽化时要吸收大量的热;
B.酸与碱、碱性氧化物等反应生成盐;
C.NH4NO3受热易分解;
D.氮气与氢气反应生成氨气,与氮气的物理性质无关.
解答 解:A.液氨汽化时要吸收大量的热,可用作制冷剂,故A错误;
B.酸与碱、碱性氧化物等反应生成盐,所以HNO3具有酸性,可用于制备硝酸盐原料,故B正确;
C.NH4NO3受热易分解,不能用于制造高温材料,制造高温材料要用高熔点的物质,与物质的溶解性无关,故C错误;
D.氮气与氢气反应生成氨气,可用于合成氨原料,与氮气的物理性质无关,故D错误.
故选B.
点评 本题考查氮的化合物的性质、用途以等知识,侧重于常识性内容的考查,难度不大,注意基础知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | 化学平衡向正向移动,反应物浓度一定降低 | |
| B. | 化学平衡向正向移动,生成物的浓度一定增加 | |
| C. | 化学平衡向正向移动,反应物的转化率一定增大 | |
| D. | 化学平衡向正向移动时,正反应速率一定大于逆反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
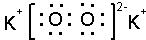 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纤维素在人体内可以水解成葡萄糖 | |
| B. | 组成蛋白质的元素中,一定含有碳、氢、氧、氮 | |
| C. | 适量摄入油脂,有助于人体吸收多种脂溶性维生素 | |
| D. | 天然蛋白质水解后的最终产物是a-氨基酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
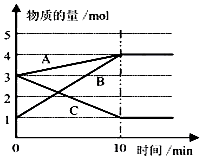 化学反应速率与限度与生产、生活密切相关
化学反应速率与限度与生产、生活密切相关| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标准状况) | 100 | 240 | 464 | 576 | 620 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ZnC2水解生成C2H2 | B. | A14C3水解生成C3H4 | ||
| C. | Mg2C3水解生成C3H4 | D. | Li2C2水解生成C2H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲酸溶液导电性比乙酸溶液导电性强,说明乙酸是弱酸 | |
| B. | 硫酸钾溶于水能导电,所以硫酸钾是电解质 | |
| C. | 强电解质一定是含有离子键,弱电解质中一定含弱极性共价键 | |
| D. | 固态磷酸是电解质,所以磷酸在熔融状态下和水溶液中都能导电 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com