
| n(H2O) |
| n(CH4) |
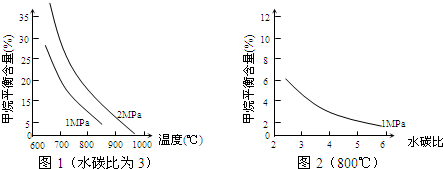
| △c |
| △t |
| c(CO)?c3(H2) |
| c(CH4)?c(H2O) |
 ;
; ;
;| △c(H2) |
| △t |
| 1.2mol/L |
| 6min |
| c(CO)?c3(H2) |
| c(CH4)?c(H2O) |
| 0.4×1.23 |
| 0.1×0.1 |


科目:高中化学 来源: 题型:
| 实验 编号 | T/K | 大理石 规格 | C(HNO3)/ mol?L-1 | 实验目的 |
| ① | 25℃ | 粗颗粒 | 2.00 | (Ⅰ) 实验①和②探究HNO3浓度对该反应速率的影响;则T1为: (Ⅱ)实验①和 (Ⅲ)实验①和 |
| ② | T1 | 粗颗粒 | 1.00 | |
| ③ | 35℃ | 粗颗粒 | 2.00 | |
| ④ | 25℃ | 细颗粒 | 2.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| pH值 | 6.5-8.5 |
| Ca2+、Mg2+总浓度 | <0.045mol/L |
| 细菌总数 | <100个?mL-1 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | T/K | 大理石规格 | HNO3浓度/mol?L-1 | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和 (Ⅲ)实验①和 |
| ② | ||||
| ③ | ||||
| ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
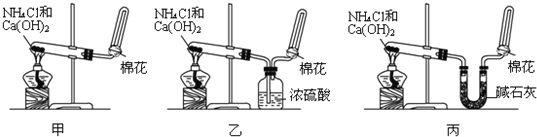
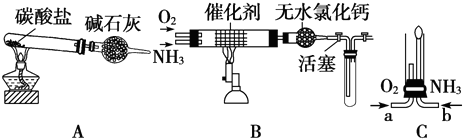
查看答案和解析>>
科目:高中化学 来源: 题型:
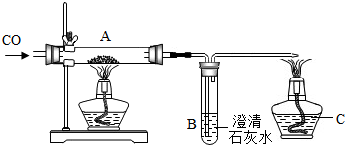 用如图装置测定某铁的氧化物中铁元素和氧元素的质量比,记录如下:
用如图装置测定某铁的氧化物中铁元素和氧元素的质量比,记录如下:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| ||

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com