
【题目】一定条件下,制备特种陶瓷的原料MgO:MgSO4(s)+CO(g)![]() MgO(s)+CO2(g)+SO2(g)ΔH>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
MgO(s)+CO2(g)+SO2(g)ΔH>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
选项 | x | y |
|
A | 温度 | 容器内混合气体的密度 | |
B | CO的物质的量 | CO2与CO的物质的量之比 | |
C | SO2的浓度 | 平衡常数K | |
D | MgSO4的质量(忽略体积) | CO的转化率 |
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
【题目】质谱显示,某有机化合物的相对分子质量为46,燃烧实验发现其分子中碳、氢原子数之比为1∶3,核磁共振谱显示,该物质中只有一种类型的氢原子。关于该化合物的描述中,正确的是( )
A.该化合物为乙醇
B.该化合物与乙醇互为同分异构体
C.该化合物为乙醚
D.该化合物与乙醚互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列3种有机化合物A:CH2=CH2、 B:CH3COOH、 C:![]()
(1)化合物B中的官能团的名称是 。
(2)能使溴的四氯化碳溶液褪色反应的化学方程式为 ;该反应类型为 。
(3)能与乙醇发生酯化反应的化学方程式为 。
(4) ![]() 在浓硫酸作用下,与浓硝酸反应的化学方程式为 。
在浓硫酸作用下,与浓硝酸反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用“键线式”简化表示。
CH3—CH=CH-CH3可简写为 ![]() 。
。
(1)有机物X的键线式为: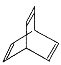 ,该有机物与H2加成时最多能消耗氢气的物质的量 ,有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式_______,将Y加入酸性高锰酸钾溶液中的现象 。
,该有机物与H2加成时最多能消耗氢气的物质的量 ,有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式_______,将Y加入酸性高锰酸钾溶液中的现象 。
(2)Y与乙烯在一定条件下发生等物质的量聚合反应,写出其反应的化学方程式:
___
(3)X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物
有 种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据氢原子和氟原子的核外电子排布,对F2和HF分子中形成的共价键描述正确的是
A.两者都为s-s σ 键
B.两者都为p-p σ 键
C.前者为p-p σ 键,后者为s-p σ 键
D.前者为s-s σ 键,后者为s-p σ 键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D为同一周期的4种元素,已知0.2 mol A与足量酸充分反应后生成2.24 L H2(标准状况下)。B的氧化物既可溶于酸又可溶于强碱溶液。C、D离子的电子层结构与氩原子相同,C点燃时与氧气反应生成的氧化物可与C的气态氢化物反应得到C的单质,D单质常温下为气态。
(1)A、B、C、D的元素名称分别为:A ,B ,C ,D 。
(2)画出B的原子结构示意图 。
(3)C在周期表中位于第 周期 族。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA 为阿伏加德罗常数的值。下列说法正确的是
A.8.7gMnO2与40mL 10mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA
B.0.1molMg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.2NA
C.由2H和18O所组成的水11g,其中所含的中子数为5NA
D.1L0.1mol·L-1Na2CO3溶液中含有的阴离子数为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com