
分析 可以根据盖斯定律来确定化学反应的焓变,物质具有的能量越低越稳定,反应物的能量大于生成物的能量,则该反应是放热反应,反之是吸热反应.常温时红磷比白磷稳定,说明白磷能量高,反应放出的热量较多;
解答 解:已知:①P4(白磷,s)+5O2(g)=2P2O5(s);△H1;
②4P(红磷,s)+5O2(g)=2P2O5(s);△H2;
②-①得到反应:4P(红磷,s)=P4(白磷,s),△H=△H2-△H1,
红磷比白磷稳定,说明红磷的能量低于白磷,所以反应4P(红磷,s)=P4(白磷,s)是吸热反应,即△H=△H2-△H1>0,常温时红磷比白磷稳定,说明白磷能量高,反应放出的热量较多,因△H<0,则放出的能量越多反应热越小,△H1<△H2,
故答案为:<.
点评 本题综合考查反应热的大小比较,题目难度不大,注意把握比较反应热的角度.


科目:高中化学 来源: 题型:解答题
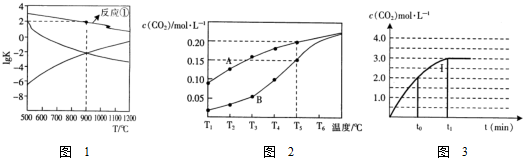
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
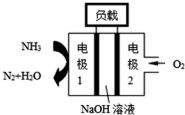 (1)已知在2L的容器中进行下列可逆反应,各物质的有关数据如下:
(1)已知在2L的容器中进行下列可逆反应,各物质的有关数据如下:| 起始物质的量浓度(mol/L) | 1.5 | 1 | 0 |
| 2s末物质的量浓度(mol/L) | 0.9 | 0.8 | 0.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.045 mol/L | B. | 1 mol/L | C. | 0.5 mol/L | D. | 2.24mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | HCl、H2SO4、NH3•H2O | B. | NaOH、HCl、H2SO4 | ||
| C. | HCl、H2SO4、NaOH | D. | HCl、NaOH、H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
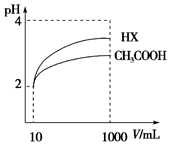 25℃时,电离平衡常数:
25℃时,电离平衡常数:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | 1.8×10-5 | K1 4.3×10-7 K2 5.6×10-11 | 3.0×10-8 | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com