
��2.0 L�����ܱ������г���1.0 mol PCl5�����¶�ΪT��ʱ�������·�ӦPCl5(g)  PCl3(g)+C12(g) ��H��+124 kJ��mol��1����Ӧ�����вⶨ�IJ������ݼ��±���
PCl3(g)+C12(g) ��H��+124 kJ��mol��1����Ӧ�����вⶨ�IJ������ݼ��±���
| ʱ��t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3��/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 |
�ش��������⣺ [��֪:Ksp(Ag3 PO4) ��1.4 �� 10��16��Ksp(AgCl) ��1.8 �� 10��10]
��1����Ӧ��ǰ50 s��ƽ������v(PCl5) �� ��������
��2���¶�ΪT��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ������������
��3��Ҫ���������Ӧ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ�ǡ�����(��дһ��)��
��4�����¶�ΪT��ʱ������ʼʱ����0.5 mol PCl5��a mol Cl2��ƽ��ʱPCl5��ת������Ϊ20������a����������
��5��PCl5����ˮ����ȫˮ������H3 PO4���÷�Ӧ�Ļ�ѧ����ʽ�ǡ������� ����0.01 mol PCl5Ͷ��l L��ˮ�У�����μ���0.1 mol /L AgNO3��Һ���Ȳ����ij����ǡ�������
��֪ʶ�㡿��ѧƽ��ļ��㣻��ѧƽ���Ӱ�����أ�
���𰸽�������1��0.0016 mol/( L��s) ��2��0.025 ��3�������¶ȡ�����ѹǿ������PCl3��Cl2��
��4��0.1 ��5��PCl5+4H2O = H3PO4+5HCl AgCl
����������1����Ӧ��ǰ50s��������0.16molPCl3�����ݷ�ӦPCl5��g��⇌PCl3��g��+Cl2��g����֪�����ĵ�PCl5�����ʵ���Ϊ0.16mol�����Է�Ӧ��ǰ50s��ƽ������v��PCl5��=0.16mol��2.0L��50s=0.0016mol•L-1•s-1��
��2���ɱ������ݿ�֪����Ӧ��250s��350sʱ���Ȼ������ʵ�����ȣ�˵��250sʱ�ﵽ��ƽ��״̬����
PCl5��g��⇌PCl3��g��+Cl2��g��
��Ӧǰ��mol�� 1.0 0 0
�仯��mol�� 0.2 0.2 0.2
ƽ��ʱ��mol�� 0.8 0.2 0.2
ƽ��ʱ����ֵ�Ũ��Ϊ��c��PCl5��=0.8mol��2.0L=0.4mol/L��c��PCl3��=c��Cl2��=0.2mol��2.0L=0.1mol/L��
���¶��¸÷�Ӧ��ƽ�ⳣ��Ϊ��K=(0.1��0.1)/0.4=0.025
��3�����ݷ�ӦPCl5��g��⇌PCl3��g��+Cl2��g����H=+124kJ•mol-1��֪������Ӧ��ת���ʣ���Ҫʹƽ�����������ƶ������������¶ȡ���Сѹǿ���������������Ȼ��ȣ�ƽ�ⶼ�����������ƶ���
��4�������¶���ͬ������ƽ�ⳣ��K=0.025��
��������ʽ�ɵã�PCl5��g��⇌PCl3��g��+Cl2��g��
��Ӧǰ��mol�� 0.5 0 a
�仯��mol�� 0.1 0.1 0.1
ƽ��ʱ��mol�� 0.4 0.1 a+0.1
ƽ��ʱ�����Ũ��Ϊ��c��PCl5��=0.2mol/L��c��PCl3��=0.05mol/L��c��Cl2��=(a+0.1)/2mol/L��
����K=0.025, ���a=0.1����5������ˮ�У����Ȼ�����ȫˮ�⣬�������ᣨH3PO4������÷�Ӧ�Ļ�ѧ����ʽΪ��PCl5+4H2O=H3PO4+5HCl��
�豥��������Һ��������Ũ��Ϊx����Ksp��Ag3P04��=x3��x/3=1.4��10-16��x= =
= ��10−4���豥���Ȼ�����Һ��������Ũ��Ϊy����y2=Ksp��AgCl��=1.8��10-10��y=
��10−4���豥���Ȼ�����Һ��������Ũ��Ϊy����y2=Ksp��AgCl��=1.8��10-10��y=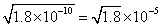 ��
��
����0.01mol PCl5Ͷ��lL��ˮ�У�����μ���AgN03��Һ���Ȳ����ij�����AgCl��
��˼·�㲦�����⿼���˻�ѧ��Ӧ���ʵļ��㡢��ѧƽ�ⳣ���ļ��㡢��ѧƽ���Ӱ�����أ���Ŀ�Ѷ��еȣ�ע�����ջ�ѧ��Ӧ���ʵı���ʽ�����㷽������ȷ��ѧƽ�ⳣ���ĸ�����㷽����


 A�ӽ��� ϵ�д�
A�ӽ��� ϵ�д� ȫ�Ų��Ծ�ϵ�д�
ȫ�Ų��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������ӽ���Ĥ�������ӽ���Ĥ��ʯī�缫�������ȼҵ�е�Ĥ����ԭ�����ش��������⡣
��1��д���ȼҵ�е�ⱥ��ʳ��ˮ�����ӷ���ʽ ��
��2�������ý���Ĥ������������ͼ��ܣ����һ�������������Һ������������Һ��������Һ��װ�ã�����������ʵĻ�ѧʽ��
A_________��C_________�� E_________��ĤbΪ ���ӽ���Ĥ�����������������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������������������������ͭ�Ļ����Һ�м������ۣ���ַ�Ӧ����ˣ���������ͭ�ۺ��������ۡ���ô��ʱ����Һ�У� ��
A���϶���Fe2+��������Fe3+ B���϶���Fe3+��������Cu2+
C���϶���Fe2+��������Fe3+��Cu2+ D��ֻ��Fe2+��û��Fe3+��Cu2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£�������Һ�и�������һ���ܴ����������
A��ʹ���ȳʺ�ɫ����Һ�У�Na+��AlO2����NO ��CO
��CO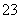
B����ˮ���������c(H+)=10��12mol��L��1����Һ��NH4+��SO42-��HCO3����Cl��
C������0.1 mol��L��1 HCO ����Һ��Na����Fe3����NO
����Һ��Na����Fe3����NO ��SCN��
��SCN��
 D�� ��0.1 mol��L��1����Һ��Na����K����CO
D�� ��0.1 mol��L��1����Һ��Na����K����CO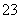 ��NO
��NO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ����
A�������£���pH��4�Ĵ�����Һϡ�ͺ���Һ���������ӵ�Ũ�Ⱦ�����
B���¶�һ��ʱ����ˮ�еμ����������γ�ϡ��Һ��ˮ�����ӻ�����Kw����
C��8NH3(g)��6NO2(g)��7N2(g)��12H2O(g) ��H��0����÷�Ӧһ�����Է�����
D������Ksp(BaSO4)��Ksp(BaCO3)����˲�����ʹBaSO4����ת��ΪBaCO3����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Cr3�����ӵĵ������������LED��ӫ��ۻ��ʲ��ϣ�������(�侧����ͼ8��ʾ)�����Ȼ����백�����෴Ӧ�Ƶá�
 |
��1����̬Cr�ļ۵����Ų�ʽ�ɱ�ʾΪ �� ��
��2���������Ļ�ѧʽΪ �� ��������ԭ������Ҿ�����ȵĵ�ԭ����ĿΪ �� ����
��3���Ȼ�������������˫����Al2Cl6�ṹ��ͼ9��ʾ����Al2Cl6�д��ڵĻ�ѧ���� �� (����ĸ)��
a�����Ӽ�������b�����ۼ�������c����λ��������d��������
��4��һ����������Al2O3��CCl4��Ӧ�Ʊ�AlCl3�ķ�ӦΪ��Al2O3��3CCl4===2AlCl3��3COCl2������COCl2���ӵĿռ乹��Ϊ �� ��һ����CCl4��Ϊ�ȵ�����ķ��ӵĻ�ѧʽΪ �� ��
��5��AlCl3��������Ӧ�������������Ӣ���̼ԭ�ӵ��ӻ�����Ϊ �� ��
 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����С�մ��dz��������ֳ�������Ʒ�����Ƕ��ǰ�ɫ���壬�����������������ʵķ�������ȷ���ǣ� ��
A���ֱ���ɰ������������Ʒ��ȫ���ֽ�ӷ�û�в��������С�մ�
B���ýྻ����˿պȡ������Ʒ��ú���ƻ��������գ�ʹ������ɫ�������Ա仯����С�մ�
C������ֻС���������ֱ����������������Ʒ���ټ��������ʳ�ף��������ݿ���Ǵ���
D���Ƚ�����������Ʒ�����Һ���ֱ�����Ȼ�����Һ���ް�ɫ�������ɵ���С�մ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ����
A��������ʴ���ǽ���ԭ��ʧȥ���ӱ���ԭ�Ĺ���
B���Ͻȴ������ױ���ʴ
C�������������ֱ����Դ�ĸ������������������ӵ������ϣ����Է�ֹ��������ʴ
D�������豸������ͭ����Է�ֹ��������ʴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ����
A��1 mol�κ�������ռ�����Լ��22.4 L
B��1 mol H2O(g)�ڱ�״�������Ϊ22.4 L
C��1 mol�������Ϊ22.4 L����һ���DZ�״��
D������Ħ�������һ����22.4 mol��L��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com