
(原创)下列物质分类正确的是
A.SO2、SiO2、P2O5均为酸性氧化物
B.是否具有丁达尔效应是胶体与溶液、浊液的根本区别
C.纯净盐酸为纯净物、冰水混合物为混合物
D.烧碱、纯碱都属于碱,油脂、甘油都属于酯
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届宁夏回族自治区银川一中高三上学期第一次月考化学试卷(解析版) 题型:选择题
化学与生产、生活密切相关。下列叙述正确的是
A.六水氯化钙可用作食品干燥剂
B.葡萄糖注射液不能产生丁达尔效应,不属于胶体
C.为改善食物的色、香、味并防止变质,可在其中加入大量食品添加剂
D.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,与肺癌等疾病的发生不相关
查看答案和解析>>
科目:高中化学 来源:2016届河南省郑州市新高三年级调研检测化学试卷(解析版) 题型:选择题
有机化合物A(C8H8O2)为一种无色液体。从A出发可发生如图的一系列反应。则下列说法正确的是
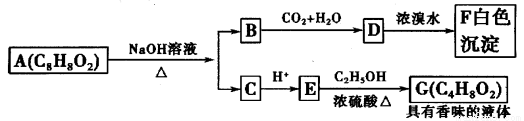
A.A的结构中含有碳碳双键
B.G的同分异构体中属于酯且能发生银镜反应的只有一种
C.上述各物质中能发生水解反应的有A、B、D、G
D.根据图示可推知D为苯酚
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三第一次月考化学试卷(解析版) 题型:填空题
(8分)(原创)用以下几种常见有机物填写下列空白:
a.CH4
b.C2H4
c.C6H6
d.C2H5OH
e.CH3COOH
(1)等质量的CH4、C2H4、C6H6三种烃完全燃烧消耗O2的量由多到少的顺序是 (用序号表示)。
(2)等物质的量混合的甲烷和乙酸蒸气完全燃烧所得二氧化碳和水蒸气的物质的量之比为 。
(3)由乙烯和乙醇蒸气组成的混合气体1mol完全燃烧所需氧气在标准状况下的体积为 L。
(4)由两种气态烃组成的混合气体完全燃烧后,将产生的气体全部通过图示装置,得到如表所列的实验数据(产生的气体完全被吸收)。
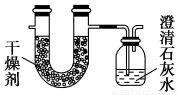
实验前 | 实验后 | |
(干燥剂+U形管)的质量 | 101.1 g | 104.7 g |
(澄清石灰水+广口瓶)的质量 | 312.0 g | 318.6 g |
根据实验数据填空:
①假设广口瓶里生成一种正盐,其质量为 g。
②混合气体中C、H两元素的物质的量之比为 。
③若混合气体是由CH4和C2H4组成,则二者的体积比为 。
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三第一次月考化学试卷(解析版) 题型:选择题
下列实验操作与对应的反应现象或原理正确的一组是
选项 | 实验操作 | 现象或原理 |
A | 取少量KI溶液,先滴加氯水,再加入少量苯,振荡、静置 | 溶液分层,下层呈紫红色 |
B | 将稀盐酸或氢氧化钠溶液慢慢滴入氢氧化铝胶体中 | 均先沉淀后溶解 |
C | 将浓硝酸加入盛有铂、金的烧杯中,不反应,加入一定量 浓盐酸后,铂、金溶解 | 浓盐酸氧化性强于浓硝酸 |
D | 将40.0 g NaOH固体溶于1.0 L蒸馏水中配成溶液 | 溶液物质的量浓度为1.0mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省忻州市高一上入学化学试卷(解析版) 题型:填空题
如图是稀盐酸和氢氧化钠溶液反应过程中溶液酸碱度的变化情况。
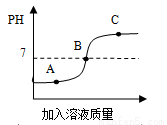
(1)该实验操作是将 滴加到另一种溶液中。
(2)A点时溶液中的溶质是 (填化学式)。
(3)右下图是反应中某时的微观图示,此时对应于上图中A、B、C中的哪一点? ;证明你的判断正确的实验操作方法是:向反应后的溶液中滴加 溶液。
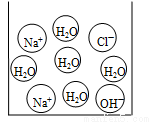
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省忻州市高一上入学化学试卷(解析版) 题型:选择题
有四种物质的溶液:①Ba(OH)2、②Na2SO4、③HNO3、④CuCl2,不用其他试剂就可将它们逐一鉴别出来,其鉴别顺序是
A.④①②③ B.①③④② C.④③②① D.①④②③
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一上学期升学化学试卷(解析版) 题型:选择题
可逆反应2NO2 2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是 ①单位时间内生成n mol O2 的同时生成2n molNO ②单位时间内生成n mol O2 的同时生成2n molNO2 ③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态 ④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态
2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是 ①单位时间内生成n mol O2 的同时生成2n molNO ②单位时间内生成n mol O2 的同时生成2n molNO2 ③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态 ④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态
A、①④ B、②④ C、①③④ D、①②③④⑤
查看答案和解析>>
科目:高中化学 来源:2016届山东省枣庄市高三9月阶段性学情检测化学试卷(解析版) 题型:填空题
硒和硫是同一主族元素,二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。完成下列填空:
(1)Se和浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1:1,写出Se和浓HNO3的反应方程式: 。
(2)已知:Se+2H2SO4(浓)→2SO2↑+SeO2+2H2O;2SO2+SeO2+2H2O→Se+2SO42-+4H+
SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是______ 。
(3)回收得到的SeO2的含量,可以通过下面的方法测定:
① SeO2+ KI+ HNO3→ Se+ I2+ KNO3+ H2O
②I2+2Na2S2O3→Na2S4O6+2NaI 配平方程式①,标出电子转移的方向和数目。
(4)实验中,准确称量SeO2样品0.1500g,消耗了0.2000 mol/L的Na2S2O3溶液25.00 mL,所测定的样品中SeO2的质量分数为___ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com