
| A、H2 |
| B、H2O |
| C、CO2 |
| D、CH4 |


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
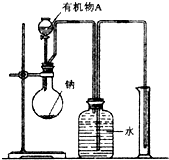 26.4g某液态有机化合物A完全燃烧后,生成21.6g H2O和52.8gCO2.测得有机化合物A的蒸气对H2的相对密度是44,求:
26.4g某液态有机化合物A完全燃烧后,生成21.6g H2O和52.8gCO2.测得有机化合物A的蒸气对H2的相对密度是44,求:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:1 | B、1:2 |
| C、1:3 | D、1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:2:3 |
| B、2:1:6 |
| C、2:1:3 |
| D、1:2:6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(H+)>1.0×10-71mol?L-1的溶液一定呈酸性 |
| B、c(H+)?c(OH-)=1.0×10-14的溶液一定呈中性 |
| C、中性溶液中的c(H+)一定等于1.0×10-71mol?L-1 |
| D、c(H+)=c(OH-)的溶液一定是中性溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、核外电子质量很小,在原子核外做高速运动 |
| B、在电子云示意图中,小黑点密表示电子在核外空间单位体积内出现的几率大 |
| C、在电子云示意图中,通常用小黑点来表示电子绕核做高速圆周运动 |
| D、s电子的原子轨道都是球形的,p电子的原子轨道都是哑铃形的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com