
·ÖĪö £Ø1£©øł¾Żn=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$”¢»Æѧ·½³ĢŹ½ÖŠ±ČĄż¹ŲĻµ2Na”«H2”ü¼ĘĖć£»
£Ø2£©ÅØĮņĖįŌöÖŲ10.8gĪŖ²śĪļĖ®µÄÖŹĮ棬øł¾ŻC2H5OH”«3H2O¼ĘĖćŅŅ“¼µÄĪļÖŹµÄĮ棬¼īŹÆ»ŅŌöÖŲ13.2gĪŖ¶žŃõ»ÆĢ¼µÄÖŹĮ棬øł¾ŻĢ¼Ō×ÓŹŲŗć¼ĘĖćCOµÄĪļÖŹµÄĮæ£¬Č»ŗóøł¾ŻŃõŌ×ÓŹŲŗć¼ĘĖćŃõĘųµÄĪļÖŹµÄĮ棻
£Ø3£©±ČŅŅ“¼¶ąŅ»øö-CH2-Ō×ÓĶŵÄĶ¬ĻµĪļĪŖ±ū“¼£®
½ā“š ½ā£ŗ£Ø1£©ÓÉĢāŅā£ŗ
2Na”«H2”ü
46g 22.4L
9.2g V£ØH2£©
V£ØH2£©=$\frac{22.4L”Į9.2g}{46g}$=4.48L£¬
¹Ź“š°øĪŖ£ŗ4.48£»
£Ø2£©øł¾ŻĒāŌ×ÓŹŲŗć£¬æÉµĆ£ŗ
C2H5OH”«3H2O
1mol 54g
n£ØC2H5OH£© 10.8g
n£ØC2H5OH£©=$\frac{1mol”Į10.8g}{54g}$=0.2mol£¬
¼īŹÆ»ŅŌöÖŲµÄÖŹĮæĪŖÉś³ÉCO2µÄÖŹĮ棬¹Źn£ØCO2£©=$\frac{13.2g}{44g/mol}$=0.3mol£¬
øł¾ŻĢ¼Ō×ÓŹŲŗć£ŗn£ØCO£©=2”Į0.2mol-0.3mol=0.1mol£¬
øł¾ŻŃõŌ×ÓŹŲŗć£ŗn£ØO2£©=$\frac{1}{2}$£Ø0.6mol+0.1mol+0.3mol”Į2-0.2mol£©=0.55mol£¬
¹Ź“š°øĪŖ£ŗ0.55£»
£Ø3£©±ČŅŅ“¼¶ąŅ»øö-CH2-Ō×ÓĶŵÄĶ¬ĻµĪļĪŖ±ū“¼£¬Ęä½į¹¹¼ņŹ½ĪŖCH3CH2CH2OHŗĶCH3CHOHCH3£»
“š£ŗ±ČŅŅ“¼¶ąŅ»øö-CH2-Ō×ÓĶŵÄĶ¬ĻµĪļµÄ½į¹¹¼ņŹ½ĪŖCH3CH2CH2OHŗĶCH3CHOHCH3£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»Æѧ·½³ĢŹ½µÄ¼ĘĖć”¢½į¹¹¼ņŹ½µÄŹéŠ“£¬²ąÖŲÓŚŅŌĪļÖŹµÄĮæĪŖÖŠŠÄµÄ¼ĘĖć¹«Ź½”¢Ō×ÓŹŲŗćµÄÓ¦ÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
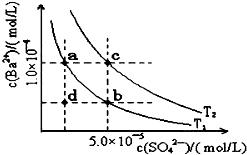 ŅŃÖŖBaSO4£Øs£©?Ba2+£Øaq£©+SO4 2-£Øaq£©£¬25”ꏱKsp=1.07”Į10-10£¬ĒŅBaSO4µÄĖęĪĀ¶ČÉżø߶ųŌö“ó£®ČēĶ¼ĖłŹ¾£¬ÓŠT1”¢T2²»Ķ¬ĪĀ¶ČĻĀĮ½ĢõBaSO4ŌŚĖ®ÖŠµÄ³ĮµķČܽāĘ½ŗāĒśĻߣ¬ŌņĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
ŅŃÖŖBaSO4£Øs£©?Ba2+£Øaq£©+SO4 2-£Øaq£©£¬25”ꏱKsp=1.07”Į10-10£¬ĒŅBaSO4µÄĖęĪĀ¶ČÉżø߶ųŌö“ó£®ČēĶ¼ĖłŹ¾£¬ÓŠT1”¢T2²»Ķ¬ĪĀ¶ČĻĀĮ½ĢõBaSO4ŌŚĖ®ÖŠµÄ³ĮµķČܽāĘ½ŗāĒśĻߣ¬ŌņĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | ĪĀ¶ČĪŖT1Ź±£¬ŌŚT1ĒśĻßÉĻ·½ĒųÓņČĪŅāŅ»µćŹ±£¬¾łÓŠBaSO4³ĮµķÉś³É | |
| B£® | Õō·¢ČܼĮæÉÄÜŹ¹ČÜŅŗÓÉdµć±äĪŖT1ĒśĻßÉĻa”¢bÖ®¼äµÄijŅ»µć | |
| C£® | ÉżĪĀæÉŹ¹ČÜŅŗÓÉbµć±äĪŖdµć | |
| D£® | T2£¾25”ę |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
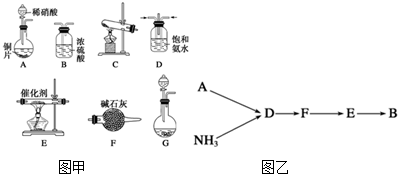
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
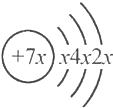 £¬bÓėcŠĪ³ÉµÄ»ÆŗĻĪļµÄ»ÆѧŹ½ĪŖb3c£¬ĒŅb”¢cĄė×ÓÓŠĻąĶ¬µÄµē×Ó²ć½į¹¹£¬ĻĀĮŠ±Č½ĻÖŠ£¬ÕżČ·µÄŹĒ£Ø””””£©
£¬bÓėcŠĪ³ÉµÄ»ÆŗĻĪļµÄ»ÆѧŹ½ĪŖb3c£¬ĒŅb”¢cĄė×ÓÓŠĻąĶ¬µÄµē×Ó²ć½į¹¹£¬ĻĀĮŠ±Č½ĻÖŠ£¬ÕżČ·µÄŹĒ£Ø””””£©| A£® | Ō×ÓŠņŹż£ŗa£¾b£¾c | B£® | Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗa£¾c£¾d | ||
| C£® | Ō×Ó°ė¾¶£ŗd£¾a£¾c | D£® | ×īøß¼Ūŗ¬ŃõĖįµÄĖįŠŌ£ŗd£¾c£¾a |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ijĪĀ¶ČŹ±£¬ŌŚŅ»øöČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ£¬X£¬Y£¬ZČżÖÖĘųĢåµÄĪļÖŹµÄĮæĖꏱ¼äµÄ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£¬øł¾ŻĶ¼ÖŠŹż¾Ż£¬ĻĀĮŠÓŠ¹ŲĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©
ijĪĀ¶ČŹ±£¬ŌŚŅ»øöČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ£¬X£¬Y£¬ZČżÖÖĘųĢåµÄĪļÖŹµÄĮæĖꏱ¼äµÄ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£¬øł¾ŻĶ¼ÖŠŹż¾Ż£¬ĻĀĮŠÓŠ¹ŲĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©| A£® | ·“Ó¦æŖŹ¼ÖĮ2min£¬ZµÄ·“Ó¦ĖŁĀŹĪŖ0.10mol•L-1•min-1 | |
| B£® | øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ3X+Y?2Z | |
| C£® | 2minŹ±£¬·“Ó¦“ļ×ī“óĻŽ¶Č£¬µ«»Æѧ·“Ó¦ČŌŌŚ½ųŠŠ | |
| D£® | ·“Ó¦“ļµ½Ę½ŗāŹ±£¬Ń¹ĒæŹĒæŖŹ¼Ź±µÄ0.9±¶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ēæ¼īŠŌČÜŅŗÖŠ£ŗK+”¢Al3+”¢Cl-”¢SO42- | |
| B£® | ŗ¬ÓŠ0.1 mol/L Fe3+µÄČÜŅŗÖŠ£ŗK+”¢Mg2+”¢I-”¢Cl- | |
| C£® | ŗ¬ÓŠ0.1 mol/L Ca2+µÄČÜŅŗÖŠ£ŗNa+”¢K+”¢SO42-”¢Cl- | |
| D£® | ŹŅĪĀĻĀ£¬pH=1µÄČÜŅŗÖŠ£ŗNa+”¢Fe3+”¢NO-3”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
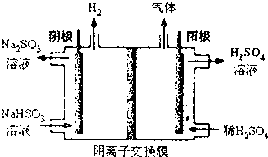 ¶ž¼×ĆŃ£ØCH3OCH4£©ŹĒŅ»ÖÖÖŲŅŖµÄĒå½ąČ¼ĮĻ£¬¹¤ŅµÉĻĄūÓĆĖ®ĆŗĘųŗĻ³É¶ž¼×ĆѵÄČż²½·“Ó¦ČēĻĀ£ŗ
¶ž¼×ĆŃ£ØCH3OCH4£©ŹĒŅ»ÖÖÖŲŅŖµÄĒå½ąČ¼ĮĻ£¬¹¤ŅµÉĻĄūÓĆĖ®ĆŗĘųŗĻ³É¶ž¼×ĆѵÄČż²½·“Ó¦ČēĻĀ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČÜŅŗÖŠČÜÓŠNaOH | B£® | ČÜÖŹæÉÄÜŹĒCu2£ØOH£©2CO3 | ||
| C£® | ČÜŅŗÖŠŅ»¶Ø²»ŗ¬ÓŠH+Ąė×Ó | D£® | ČÜŅŗ³Ź¼īŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | »īŠŌĢ攢C60”¢½šøÕÉ°¶¼ŹĒĢ¼µÄĶ¬ĖŲŅģŠĪĢå | |
| B£® | Fe2O3”¢Na2O2”¢K2O¶¼ŹĒ¼īŠŌŃõ»ÆĪļ | |
| C£® | µķ·Ū”¢µ°°×ÖŹ”¢ÓĶÖ¬¶¼ŹōÓŚÓŠ»śøß·Ö×Ó»ÆŗĻĪļ | |
| D£® | “æ¼ī”¢ĀČ»Æļ§”¢Ć÷·Æ¶¼ŹĒŃĪĒŅ¶¼ŹōÓŚĒæµē½āÖŹ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com