
下列关于胶体的说法中正确的是( )
A.溶液和胶体的本质区别是当一束光线通过胶体时可出现一条光亮的通路,溶液则没有此现象
B.制备Fe(OH)3胶体的方法是将饱和氯化铁溶液加热煮沸
C.静电除尘,利用了胶体电泳
D.胶体不均一、不稳定,静置易产生沉淀;溶液均一、稳定,静置不产生沉淀
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
分子组成为C9H12的苯的同系物,已知苯环上只有一个取代基,下列说法中正确的是( )
A.该有机物不能发生加成反应,但能发生取代反应
B.该有机物不能使KMnO4酸性溶液褪色,但能使溴水褪色
C.该有机物分子中的所有原子可能在同一平面上
D.该有机物的一溴代物最多有6种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
使用容量瓶配制溶液时,由于操作不当,会引起误差,下列情况会使所配溶液浓度偏低的是( )
①使用天平(使用游码)称量时,被称量物与砝码位置放颠倒了
②用滴定管量取液体时,开始时平视读数,结束后俯视读数
③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
④转移溶液前容量瓶内有少量蒸馏水
⑤定容时,仰视容量瓶刻度线
 ⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
A.①③⑤⑥ B.①②⑤⑥
C.②③④⑥ D.③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
50 g镁、锌、铝的混合物与适量的稀硫酸反应,得三种盐的混合溶液,然后加热、蒸发、结晶得晶体(不含结晶水)218 g,则反应中得H2的质量为( )
A、2 g
B、3 g
C、3.5 g
D、4.5 g
查看答案和解析>>
科目:高中化学 来源: 题型:
向 镁和铝的混合物重加入适量的稀硫酸,恰好完全反应生成标准状况下的气体
镁和铝的混合物重加入适量的稀硫酸,恰好完全反应生成标准状况下的气体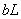 。向反应后的溶液中加入
。向反应后的溶液中加入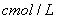 氢氧化钾溶液
氢氧化钾溶液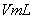 ,使金属离子刚好沉淀完全,得到的沉淀质量为ng。再将得到的沉淀灼烧至质量不再改变为止,得到固体
,使金属离子刚好沉淀完全,得到的沉淀质量为ng。再将得到的沉淀灼烧至质量不再改变为止,得到固体 。则下列关系不正确的是( )
。则下列关系不正确的是( )
A、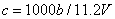
B、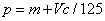
C、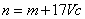
D、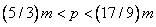
查看答案和解析>>
科目:高中化学 来源: 题型:
 2010年诺贝尔物理学奖用于表彰首次剥离出单层石墨的科学家。单层石墨称为石墨烯,这种“只有一层碳原子厚的碳薄片”的石墨烯,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,应用前景十分广阔,下列关于石墨烯的叙述正确的是( )
2010年诺贝尔物理学奖用于表彰首次剥离出单层石墨的科学家。单层石墨称为石墨烯,这种“只有一层碳原子厚的碳薄片”的石墨烯,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,应用前景十分广阔,下列关于石墨烯的叙述正确的是( )
A.石墨烯是碳单质
B.石墨烯是一种有机物
C.石墨烯中碳原子的化合价为+3
D.石墨烯可导电,说明它是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
分类方法在化学学科的发展中起到重要的作用。下列分类标准合理的是( )
A.根据纯净物的元素组成,将纯净物分为单质和化合物
B.根据溶液导电能力强弱,将电解质分为强电解质、弱电解质
C.根据分散质粒子直径的大小,将分散系分为溶液、浊液和胶体
D.根据反应中的能量变化,将化学反应分为“化合、分解、复分解、置换”四类
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定。
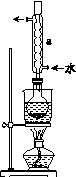
Ⅰ.制备Na2S2O3·5H2O
反应原理:Na2SO3(aq)+S(s)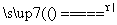 Na2S2O3(aq)
Na2S2O3(aq)
实验步骤:
①称取15 g Na2SO3加入圆底烧瓶中,再加入80 mL蒸馏水。另取5 g研细的硫粉,用3 mL乙醇润湿,加入上述溶液中。
②安装实验装置(如图所示,部分夹持装置略去),水浴加热,微沸60 min。
③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O3·5H2O,经过滤、洗涤、干燥,得到产品。
回答问题:
(1)硫粉在反应前用乙醇润湿的目的是__________________________。
(2)仪器a的名称是________,其作用是____________________。
(3)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是______________。检验是否存在该杂质的方法是____________________________。
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子反应方程式表示其原因:________________________________________________________________________
________________________________________________________________________。
Ⅱ.测定产品纯度
准确称取W g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.100 0 mol·L-1碘的标准溶液滴定。
反应原理为2S2O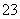 +I2===S4O
+I2===S4O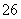 +2I-
+2I-
(5)滴定至终点时,溶液颜色的变化:____________________________________________。
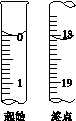
(6)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为__________mL。产品的纯度为(设Na2S2O3·5H2O相对分子质量为M)______________。
Ⅲ.Na2S2O3的应用
(7)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO ,常用作脱氯剂,该反应的离子方程式为____________________________________________。
,常用作脱氯剂,该反应的离子方程式为____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列情况能发生消去反应的是( )
A.1-溴丙烷与NaOH醇溶液共热
B.氯乙烷与NaOH的水溶液共热
C.乙醇与浓H2SO4共热至140℃
D.乙醇与浓H2SO4共热至170℃
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com