
【题目】根据要求回答下列问题:
I. ①H、D、T ②H2O、D2O ③石墨、金刚石 ④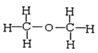 和
和 ⑤
⑤
四组微粒或物质中,互为同位素的是_______;(填序号,下同)互为同素异形体的是_____;互为同分异构体的是_____。
II.现有①金刚石 ②干冰 ③Na2SO4 ④NH4Cl 四种物质,按下列要求回答:
(1)晶体熔化时需要破坏共价键的是_____(填序号,下同);
(2)熔点最低的是_______;
(3)晶体中只存在一种微粒作用力是_______;
(4)属于离子晶体的是________。
【答案】① ③ ④ ① ② ① ③④
【解析】
I.同位素是质子数相同、中子数不同的原子互称同位素;
同素异形体是同种元素组成的不同性质的单质;
同分异构体是分子式相同结构不同的化合物;
II.原子晶体是由原子通过共价键结合而成;离子晶体是离子间通过离子键结合成;分子晶体构成微粒是分子通过分子间作用力结合而形成;微粒间作用力大小关系一般为原子晶体>离子晶体>金属晶体>分子晶体,据此分析解答。
I.①H、D、T是质子数相同、中子数不同的原子,三者互为同位素;
③石墨、金刚石是C元素构成的不同性质的单质,二者互为同素异形体;
④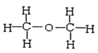 和
和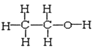 中前者是二甲醚,后者是乙醇,二者分子式都是C2H6O,结构不同,二甲醚和乙醇二者互为同分异构体;
中前者是二甲醚,后者是乙醇,二者分子式都是C2H6O,结构不同,二甲醚和乙醇二者互为同分异构体;
II.①金刚石是由C原子通过共价键结合而形成的空间网状结构的原子晶体,由于共价键结合力很强,断裂消耗很高能量,因此熔沸点高,硬度大;
②干冰是固体CO2,由CO2分子通过分子间作用力结合形成的分子晶体,分子间作用力很弱,因此熔沸点低,硬度小;
③Na2SO4是由Na+、SO42-通过离子键结合形成的离子晶体,在阴离子SO42-中存在共价键;离子键比共价键结合力弱,但比分子间作用力大很多;
④NH4Cl是由NH4+、Cl-通过离子键结合形成的离子晶体,在阳离子NH4+中存在共价键,晶体熔化断裂离子键。
综上所述可知(1)晶体熔化时需要破坏共价键的是①;
(2)熔点最低的是②;
(3)晶体中只存在一种微粒作用力是①;
(4) 属于离子晶体的是③④。


科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)![]() 2SO3(g) △H<O,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g) △H<O,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是

A. 图I研究的是t0时刻增大O2的浓度对反应速率的影响
B. 图II研究的是t0时刻增大压强后对反应速率的影响
C. 图III研究的是催化剂对化学平衡的影响,且甲的催化效率比乙高
D. 图III研究的是温度对化学平衡的影晌.且乙的温度较高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下图所示的装置中,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极质量增大,则以下叙述正确的是
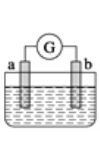
A. a为正极,是碳棒,烧杯中的溶液为硫酸
B. b为负极,是铁片,烧杯中的溶液为硫酸铜溶液
C. 外电路的电子流向为:b→外电路→a
D. 溶液中阳离子向a 极移动,且a极上发生的是氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各图是表示相应变化的能量关系图,其中正确的是( )
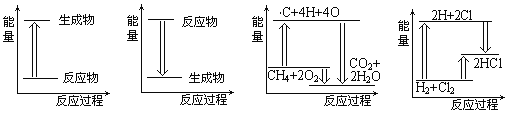
A. 锌与稀硫酸的反应 B. 植物的光合作用 C. 天然气燃烧 D. H2与Cl2反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素化合价的说法正确的是
A.主族元素的最高正价均等于其族序数
B.非金属元素的最低负价均等于最高正价8
C.金属元素无负价、氟元素无正价
D.氯元素只有1、+1、+5、+7四种价态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。
(1)已知甲烷和汽油(可用 C8H18表示)的燃烧的热化学方程式:
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890kJ/mol;
C8H18(l)+![]() O2(g)═8CO2(g)+9H2O(l)△H=﹣5472kJ/mol;
O2(g)═8CO2(g)+9H2O(l)△H=﹣5472kJ/mol;
则等质量的甲烷和汽油燃烧,产生的热量比较多的是___________(填“甲烷”或“汽油”)
(2)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成 SiO2和液态 H2O。已知室温下 2gSiH4自燃放出热量 89.2kJ.SiH4自燃的热化学方程式为____________________.
(3)1molH2(g)和1mol Cl2(g)在一定条件下反应生成2 mol HCl(g),放出184.5kJ的热量,已知断裂1molH2(g)中的H-H和1mol Cl2(g)中的Cl-Cl分别需要吸收436.4kJ和242.7kJ的能量,则1mol HCl分子中的化学键形成时释放_________kJ的能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,进行下列反应. 2A(g)+B(g)+C(s) ![]() D(g)+E(g)(正反应吸收热量)达到平衡后,下列说法中正确的是( )
D(g)+E(g)(正反应吸收热量)达到平衡后,下列说法中正确的是( )
A. 若恒温定容情况下,充入一些稀有气体压强增大,E的物质的量将不变
B. 若恒温定压条件下,加入C(s),则B的转化率将增大
C. 若定容升温,在新平衡体系中气体平均相对分子质量将减小
D. 在温度、压强和容积都相同时,在另一密闭容器中加入2 mol A、1 mol B、1 molC,平衡时两个容器中D和E的浓度分别相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com