
【题目】升高温度,下列数据不一定增大的是
A. 水的离子积常数B. 化学平衡常数C. 反应的活化分子百分数D. 化学反应速率
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A.28g氮气所含有的原子数目为NA
B.标准状况下,22.4L水中含有个水分子NA
C.2NA个氯气的体积是NA个氧气的体积的2倍
D.标准状况下,22.4L氯化氢所含的原子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去溶液中的NaCl和Na2SO4,从而得到纯净的NaNO3溶液。相应的实验过程可用下图表示:

请回答下列问题:
(l)写出实验流程中下列物质的化学式:试剂X_______,沉淀A_______。
(2)上述实验流程中加入过量的Na2CO3的目的是_______。
(3)按此实验方案得到的溶液3中肯定含有_______(填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的_______,之后若要获得固体NaNO3需进行的实验操作是_______(填操作名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列图象的分析错误的是( )
A. 图可表示对平衡N2(g)+3H2(g)2NH3(g)加压、同时移除部分NH3时的速率变化
图可表示对平衡N2(g)+3H2(g)2NH3(g)加压、同时移除部分NH3时的速率变化
B.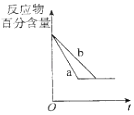 图中a、b曲线只可表示反应H2(g)十I2(g)2HI(g)在有催化剂和无催化剂存在下建立平衡的过程
图中a、b曲线只可表示反应H2(g)十I2(g)2HI(g)在有催化剂和无催化剂存在下建立平衡的过程
C. 图表示向CH3COOH溶液中逐渐加入CH3COONa固体后,溶液pH的变化
图表示向CH3COOH溶液中逐渐加入CH3COONa固体后,溶液pH的变化
D. 图表示向醋酸溶液中加水时其导电性变化,则CH3COOH溶液的pH:a<b
图表示向醋酸溶液中加水时其导电性变化,则CH3COOH溶液的pH:a<b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题:
(1)纯水在T℃时,pH=6,该温度下1molL﹣1的NaOH溶液中,由水电离出的c(OH﹣)=molL﹣1 .
(2)某一元弱酸溶液(A)与二元强酸(B)的pH相等.若将两溶液稀释相同的倍数后,pH(A)pH(B) (填“>”、“=”或“<”).现用上述稀释溶液中和等浓度等体积的NaOH溶液,则需稀释溶液的体积V(A)V(B)(填“>”、“=”或“<”).
(3)已知:二元酸H2R 的电离方程式是:H2R=H++HR﹣ , HR﹣R2﹣+H+ , 若0.1molL﹣1NaHR溶液的c(H+)=a molL﹣1 , 则0.1molL﹣1H2R溶液中c(H+)(0.1+a) molL﹣1(填“<”、“>”或“=”),理由是 .
(4)电离平衡常数是衡量弱电解质电离程度的物理量.已知:
化学式 | 电离常数(25℃) |
HCN | K=4.9×10﹣10 |
CH3COOH | K=1.8×10﹣5 |
H2CO3 | K1=4.3×10﹣7、K2=5.6×10﹣11 |
①25℃时,有等浓度的HCN溶液、H2CO3溶液和CH3COOH溶液,三溶液的pH由大到小的顺序为(用化学式表示).
②向NaCN溶液中通入少量的CO2 , 发生反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子反应,表达正确的是( )
A. 向KHSO4溶液中加入Ba(OH)2溶液至溶液呈中性:2H+ + SO42-+ Ba2+ + 2OH-= BaSO4↓ + 2H2O
B. CaCO3与醋酸反应:CaCO3 + 2H+=Ca2+ + CO2↑+ H2O
C. 向碳酸氢钙溶液中滴入过量澄清石灰水:Ca2++2HCO3—+2OH— =CaCO3↓+CO32—+2H2O
D. MgSO4溶液跟Ba(OH)2溶液反应:SO42― + Ba2+=BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关铁的叙述中,不正确的是( )
A.铁具有良好的延展性、导电性、导热性
B.铁的化学性质非常不活泼
C.在化学反应中,铁能生成+2价或+3价的化合物
D.铁是钢的主要成份,钢铁是主要的金属材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有的离子如下表所示:
可能大量含有的阳离子 | H+、Mg2+、Al3+、NH4+、Fe3+ |
可能大量含有的阴离子 | Cl-、NO3-、SO42-、CO32-、AlO2- |
为探究其成分,进行了探究实验。取一定量的溶液,向其中逐滴加入氢氧化钠溶液,产生沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)的关系如图所示:

(1)该溶液中一定不存在的阳离子是_____________
(2)该溶液中一定不存在的阴离子是_____________
(3)该溶液中含有的阳离子其对应的物质的量浓度之比为____________________________
(4)写出沉淀减少过程中发生反应的离子方程式____________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com