
根据已学知识,请你回答下列问题:
(1)含有8个质子,10个中子的原子的化学符号__________。
(2)最外层电子排布为4s24p1的原子的核电荷数为__________。
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布是4s24p4,该元素的名称是_________。
(4)根据VSEPR模型,H3O+的分子立体结构为: ,SO2的立体结构为: 。
(5)周期表中最活泼的非金属元素原子的轨道表示式为__________ 。
( 6 ) 三氯化铁常温下为固体,熔点282°C,沸点315°,在300°C以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体为________。
( 7 ) 某元素核外有三个电子层,最外层电子数是核外电子总数的1/6,写出该元素原子的电子排布式是__________。
( 8 )写出铬元素在周期表中的位置__________,它位于__________区。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A. 乙烯和乙烷都能发生加聚反应
乙烯和乙烷都能发生加聚反应
B.蛋白质水解的最终产物是多肽
C.米酒变酸的过程涉及了氧化反应
D.石油裂解和油脂皂化都有高分子生成小分子的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
有以下实验装置可供选择
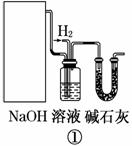 | 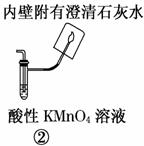 |
实验室用甲醇催化氧化法得到甲醛,并验证甲醛的性质。请回答下列问题:
(1)应选择的装置是________(填写编号);
(2)若③硬质玻璃管中装有铜粉,请写出硬质玻璃管中发生反应的化学方程式________________________________________________________________________;
(3)实验结束后,观察到溴水褪色。为解释这一现象,某学习小组的同学提出两种猜想:
A.发生了加成反应; B.发生了氧化反应。
为探究哪种猜想正确,学习小组的同学用pH计测溴水褪色前后溶液的pH,测得溶液的pH下降,你认为发生何种反应,请说出你的理由__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于晶体的叙述错误的是( )
A.在金刚石网状结构中,由共价键形成的最小碳环上有6个碳原子
B.在氯化钠晶体中,每个钠离子的周围与它最近且等距离的钠离子有12个
C.在干冰晶体中,每个二氧化碳分子周围距离最近且相等的二氧化碳分子数是12
D.在氯化铯的晶体中,每个铯离子的周围与它最近且等距离的铯离子有8个
查看答案和解析>>
科目:高中化学 来源: 题型:
实验测得BeCl2为共价化合物,两个Be—Cl键间的夹角为180°,以下判断正确的是( )
A.由极性键构成的极性分子 B.由极性键构成的非极性分子
C.由非极性键构成的极性分子 D.BeCl2中Be采取sp2杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质分类正确的是 ( )
A.苯和溴苯均为芳香烃 B.酚醛树脂和聚乙烯均为体型高分子材料
C.葡萄糖和麦芽糖均为还原性糖 D.油脂和淀粉均为天然高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
根据表1信息,判断以下叙述正确的是( )
表1 部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
 A.氢化物的沸点为H2T<H2R B.单质与稀盐酸反应的速率为L<Q
A.氢化物的沸点为H2T<H2R B.单质与稀盐酸反应的速率为L<Q
C.M与T形成的化合物具有两性 D.L2+与R2-的核外电子数相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com