
【题目】下列有关有机物的叙述正确的是( )
A.煤井中的瓦斯气和家庭使用的液化石油气的主要成分都是甲烷
B.苯的结构简式为 ![]() ,分子式可简化为CH
,分子式可简化为CH
C.利用酸性KMnO4溶液可鉴别乙烯和乙烷
D.苯与乙烯均能与溴水发生加成反应,而甲烷只能与溴水发生取代反应
科目:高中化学 来源: 题型:
【题目】对于周期表中下列位置的①~⑩十种元素,根据有关要求回答:
(1)能形成共价键的元素共有种。
(2)只需形成一个共价单键就能达到稳定结构的元素有(填元素符号)。
(3)气态氢化物溶于水生成的呈碱性的化合物是(填化学式)。
(4)⑩号元素最高正价含氧酸只含有键。
(5)①⑤⑦形成的化合物的电子式为。
(6)某元素的气态氢化物为H2B,其最高价氧化物中B的质量分数为40%,则其气态氢化物的电子式为 , 它与③的化合物的分子式为 , 含有的化学键类型有。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. CO、NO、NO2都是大气污染气体,在空气中都能稳定存在
B. NH3汽化时吸收大量的热,因此,氨常用作制冷剂
C. CO2、NO2或SO2都会导致酸雨的形成
D. 活性炭、SO2、Na2O2都能使品红溶液褪色,原理不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置应用于实验室制氯气并回收氯化锰的实验,已知氯化锰可溶于水,二氧化锰难溶于水,能达到实验目的的是:( )
A.用装置甲制取氯气
B.用装置乙吸收实验过程中制取的多余的氯气
C.用装置丙分离二氧化锰和氯化锰溶液
D.用装置丁除去氯气中的少量氯化氢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种物质有如下变化关系,E是淡黄色粉末,判断:
(1)写出A、B、C、D、E、F的化学式:
A.;B.;C.;
D.;E.;F.。
(2)写出有关反应的化学方程式(是离子反应的直接写出离子方程式)
B → C: ,
E → B: ,
C → F: ,
F → C:。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组制备氢氧化亚铁沉淀.
实验1 |
| 实验现象 |
液面上方产生白色絮状沉淀,迅速变为灰绿色,振荡,试管壁上有红褐色沉淀生成. |
(1)实验1中产生白色沉淀的离子方程式是 .
(2)为了探究沉淀变灰绿色的原因,该小组同学展开如下探究: ①甲同学推测灰绿色物质为Fe(OH)2和Fe(OH)3混合物.查阅资料后根据调色原理认为白色和红褐色的调和色不可能是灰绿色,并设计实验证实灰绿色物质中不含有Fe(OH)3 , 方案是 .
②乙同学查阅文献:Fe(OH)2在大量SO42﹣存在的情况下形成Fe6(SO4)2(OH)4O3(一种氧基碱式复盐).并设计对比实验证实该假设:向试管中加入 , 再往试管中加入 , 振荡,现象与实验1相同,结论是该假设不成立.
③乙同学继续查阅文献:Fe(OH)2沉淀具有较强的吸附性能,灰绿色可能是由Fe(OH)2表面吸附Fe2+引起.推测所用的硫酸亚铁溶液的浓度应越小越好;氢氧化钠溶液浓度应越大越好.设计了如下实验方案:
试管中10mL | 滴加 | 实验现象 | |
实验2 | 6mol/L | 0.2mol/L FeSO4溶液 | 产生悬浮于液面的白色沉淀(带有少量灰绿色),沉淀下沉后,大部分灰绿色变为白色沉淀 |
实验3 | 6mol/L | 0.1mol/L FeSO4溶液 | 产生悬浮于液面的白色沉淀(带有极少量灰绿色),沉淀下沉后,底部都为白色沉淀 |
该实验得出的结论是 , 能说明灰绿色是由Fe(OH)2表面吸附Fe2+引起的证据是 . 丙同学认为该实验方案不足以证明灰绿色是由Fe(OH)2表面吸附Fe2+引起的,还需补充的实验是 , 证明该假设成立.
(3)丙同学探究温度对氢氧化亚铁制备实验的影响:取少量灰绿色沉淀,在水浴中加热,颜色由灰绿变白,且有絮状白色沉淀下沉,原因为 .
(4)根据以上实验探究,若尽可能制得白色Fe(OH)2沉淀,需要控制的实验条件 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用高锰酸钾制取氧气时有如下操作步骤:①加热②检查装置的气密性③装药品④用排水集气法收集⑤从水槽中取出导气管⑥熄灭酒精灯⑦连接仪器。其中操作顺序正确的是( )
A. ①⑦③②⑤④⑥ B. ⑦②③①④⑤⑥
C. ⑤⑦③②①④⑥ D. ⑦③①②④⑥⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组对某品牌牙膏中摩擦剂的成分及其含量进行以下探究:
查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体生成。利用下图所示装置(夹持仪器略去),对该牙膏样品中碳酸钙的含量进行定量测定。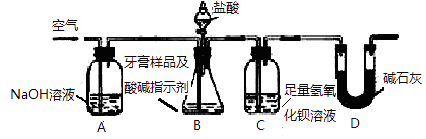
(1)C中反应生成BaCO3的化学方程式是
(2)装置D的作用是
(3)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:
(4)下列各项措施中,不能提高测定准确度的是(填标号)。
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A→B之间增添盛有浓硫酸的洗气装置
d.在B→C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)实验中准确称取10.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g 。则样品中碳酸钙的质量分数为
(6)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组在研究Na2SO3溶液、FeCl3溶液性质及反应时,进行了下列实验:
(1)取1molL﹣1的Na2SO3溶液置于空气中,测得其pH随时间的变化曲线如图所示: 
①最初,Na2SO3溶液pH=7.8,解释其原因的离子方程式是 .
②t时间段内,造成其pH发生上述变化,用离子方程式解释是 .
(2)探究Na2SO3溶液与FeCl3溶液实际反应的情况: 实验ⅰ
装置 | 操作 | 现象 |
| 向2mL1molL﹣1FeCl3溶液中,逐滴滴加1moL﹣1Na2SO3溶液2mL | 溶液黄色逐渐加深,最终得红褐色溶液(W) |
实验ⅱ
装置 | 操作 | 现象 |
| 取1mL溶液W于试管中,向其滴加过量盐酸,再滴加5滴BaCl2溶液 | 产生白色沉淀 |
①实验ⅱ证明,溶液中含有离子;
②对Na2SO3溶液与FeCl3溶液实际反应存在两种认识:
认识Ⅰ.反应中Fe3+完全转化为Fe2+ , W溶液中c(Fe2+)一定很大,反应的离子方程式是 .
认识Ⅱ.W溶液中c(Fe2+)应该极小,否则W溶液不会呈红褐色.
(3)资料显示:Fe2+呈淡绿色、FeSO3是墨绿色沉淀、碱式硫酸铁[Fe4(OH)2(SO4)5]溶液为红褐色. ①实验中始终未出现墨绿色沉淀,说明c(Fe2+)极小,其原因用离子方程式解释是 .
②实验过程和结果显示,O2、Fe3+、SO42﹣的氧化性强弱顺序是 .
③若Fe4(OH)2(SO4)5是造成溶液W呈红褐色的原因之一,其形成的化学方程式是 .
④用激光笔照射W溶液,发现有丁达尔现象,用离子方程式解释原因是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com