
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.14gC2H4含有的单键数目为3NA
B.99℃时,1LpH=6的纯水中,含有的OH-数目为1×10-8NA
C.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA
D.100 g CaS与CaSO4的混合物中含有32 g硫,则含有的氧原子数为1.75NA
【答案】D
【解析】
A.14gC2H4的物质的量是0.5mol,由于在1个乙烯分子在含有4个C-H共价单键,所以0.5mol乙烯分子中含有的单键数目为2NA,A错误;
B.根据99℃水的pH可知:此时水电离产生的c(H+)=c(OH-)=10-6mol/L,所以99℃时,1LpH=6的纯水中,所含有的OH-数目为1×10-6NA,B错误;
C.缺少溶液的体积,不能计算微粒的数目,C错误;
D.32gS的物质的量是1mol,100 g CaS与CaSO4的混合物中含有32 g硫,则混合物的摩尔质量是M=100g/mol,假设含有CaS物质的量是x,CaSO4物质的量是y,则x+y=1,72x+136y=100,解得x=![]() ,y=
,y=![]() ,则含有的氧原子数为
,则含有的氧原子数为![]() ×4×NA=1.75NA,D正确;
×4×NA=1.75NA,D正确;
故合理选项是D。


科目:高中化学 来源: 题型:
【题目】“84消毒液”是一种以NaClO为主的高效消毒剂,被广泛用于宾馆、旅游、医院、食品加工行业、家庭等的卫生消毒,某“84消毒液”瓶体部分标签如图1所示,该“84消毒液”通常稀释100倍(体积之比)后使用,请回答下列问题:
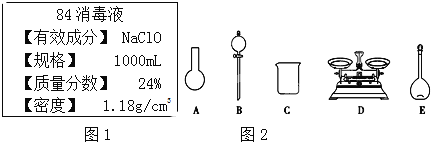
(1)此“84消毒液”的物质的量浓度约为______mol/L(计算结果保留一位小数)。
(2)某同学量取此“84消毒液”,按说明要求稀释后用于消毒,则稀释后的溶液中c(Na+)=___mol/L。
(3)该同学参阅读该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为24%的消毒液。
①如图2所示的仪器中配制溶液需要使用的是______(填仪器序号),还缺少的玻璃仪器是_______。
②下列操作中,容量瓶不具备的功能是_____(填仪器序号)。
a.配制一定体积准确浓度的标准溶液 b.贮存溶液
c.测量容量瓶规格以下的任意体积的溶液 d.准确稀释某一浓度的溶液
e.用来加热溶解固体溶质
③请计算该同学配制此溶液需称取称量NaClO固体的质量为______g。
(4)若实验遇下列情况,导致所配溶液的物质的量浓度偏高是______。(填序号)。
A.定容时俯视刻度线 B.转移前,容量瓶内有蒸馏水
C.未冷至室温就转移定容 D.定容时水多用胶头滴管吸出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组进行了有关Cu、硝酸、硫酸化学性质的实验,实验过程如下图所示。下列有关说法正确的是
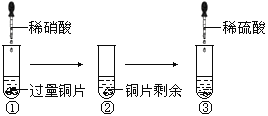
A. 实验①中溶液呈蓝色,试管口有红棕色气体产生,说明稀硝酸被Cu还原为NO2
B. 实验③中滴加稀硫酸,铜片继续溶解,说明稀硫酸的氧化性比稀硝酸强
C. 实验③发生反应的化学方程式为:3Cu+Cu(NO3)2+4H2SO4=4CuSO4+2NO↑+4H2O
D. 由上述实验可得出结论:Cu在常温下既可以和稀硝酸反应,也可以和稀硫酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列十种物质:①液态氯化氢;②小苏打;③固体纯碱;④二氧化碳;⑤葡萄糖;⑥氢氧化钾;⑦氢氧化铁胶体;⑧氨水;⑨空气;⑩硫酸铁溶液。
(1)上述十种物质中,属于电解质的___________,属于非电解质的有____________。
(2)有两种物质在水溶液中可发生反应,离子方程式为:H+ + OH- = H2O,该反应的化学方程式为________。
(3)除去③中少量②的操作是___________,化学方程式为__________。
(4)现有10mL⑩溶液中含Fe3+ 5.6g,则溶液中SO42-的物质的量浓度是____________。
(5)若在⑦中缓慢加入①的水溶液,产生的现象是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究,其结构简式如图。下列关于分枝酸的叙述不正确的是( )
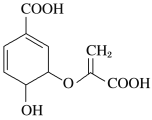
A. 分子中含有4种官能团
B. 可与乙醇、乙酸反应,且反应类型相同
C. 1 mol 分枝酸最多可与2 mol NaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由SO2和O2制备SO3(熔点16.8 ℃,沸点44.8 ℃)的模拟装置如图所示(加热和夹持装置省略):
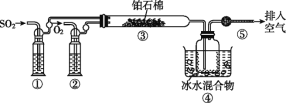
下列说法正确的是( )
A.装置①中的试剂为饱和NaHSO3溶液
B.实验室可用铜与浓硫酸在常温条件下制取SO2
C.装置③反应管中的铂石棉用作反应的催化剂
D.从装置⑤逸出的气体有过量的SO2和O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2FeSO4·7H2O ![]() Fe2O3+SO2↑+SO3↑+14H2O↑。用下图所示装置检验FeSO4·7H2O的所有分解产物,下列说法不正确的是
Fe2O3+SO2↑+SO3↑+14H2O↑。用下图所示装置检验FeSO4·7H2O的所有分解产物,下列说法不正确的是
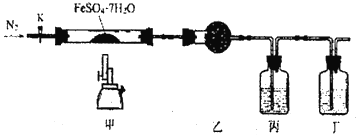
A. 乙、丙、丁中可依改盛装无水CuSO4、Ba(NO3)2溶液、品红溶液
B. 实验时应先打开K,缓缓通入N2,再点燃酒精喷灯
C. 甲中残留固体加稀硫酸溶解,再滴加KSCN,溶液变红
D. 还应在丁装置后面连接盛有NaOH溶液的洗气瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有如下转化关系(其他产物及反应所需条件均已略去)。
![]()
以下推断错误的是
A.当X是盐酸时,则F可能是稀硫酸
B.当X是氢氧化钠时,则D是红棕色气体
C.当X是不论是盐酸还是氢氧化钠时,则F都可能是强酸
D.当X是氢氧化钠时,B跟Cl2反应可能有白烟现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe2O3、Cu2O都是红色粉末,常用作颜料。某校化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物。探究过程如下:
查阅资料:Cu2O溶于稀硫酸生成Cu和CuSO4;在空气中加热生成CuO.
提出假设:
假设1:红色粉末是Fe2O3
假设2:______.
假设3:红色粉末是Cu2O和Fe2O3
(1)设计探究实验:取少量粉末放入足量稀硫酸中,在所得溶液中再滴加KSCN溶液。
(2)若假设1成立,则实验现象是______.
(3)若滴加KSCN试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁。你认为这种说法合理吗?______.简述你的理由______.
(4)若固体粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红色,则证明假设______成立
(5)实验小组欲用加热法测定Cu2O的质量分数。取ag固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为______.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com