
| A. | 用小苏打治疗胃酸过多 | |
| B. | 生石灰作食品干燥剂 | |
| C. | 打磨磁石制指南针 | |
| D. | 酸性重铬酸钾检验司机是否酒后驾车 |
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温常温下,0.1molH2O2中含有极性共价键的数目为0.1NA | |
| B. | 电解饱和食盐水时,当阴极产生22.4LH2时,电路中转移的电子数为2NA | |
| C. | 100mL12mol•L-1的浓HNO3与过量Cu反应转移电子的数目为0.6NA | |
| D. | 标准状况下,11.2L由CH4和C2H4组成的混合气体中含有氢原子的数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
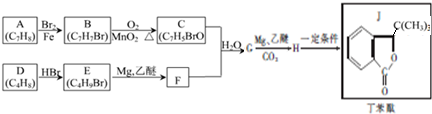
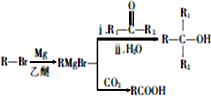
 .
.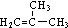 +HBr→(CH3)3CBr.
+HBr→(CH3)3CBr.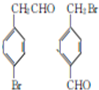 .
.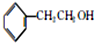 )
) .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | n+3 | B. | n+4 | C. | n-6 | D. | n-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O.1mol/LKHC03溶液与O.1mol/L KOH溶液等体积混合,所得溶液中:c(K+)>c(CO32-)>c(HCO3-)>c(OH-) | |
| B. | pH=1的NaHSO4溶液:c(H+)═c(SO42-)+c(OH-) | |
| C. | 20ml O.lmol/L CH3COONa溶液与lOmLO.lmol/L HCl溶液混合后溶液呈酸性,所得溶液中:C(Cl-)>(CH3COO-)>c(H+)>c(CH3COOH) | |
| D. | pH=2的H2C2O4溶液与pH=l2的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH-)+c(HC2O4-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
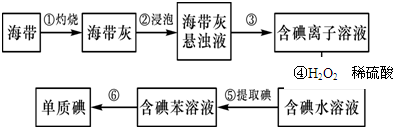
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com