
利用下列反应可以将粗镍转化为纯度达99.9%的高纯镍。

下列说法错误的是
A.对于反应一,适当增大压强,有利于Ni(CO)4的生成
B.提纯过程中,CO气体可循环使用
C.升高温度,反应一的反应速率减小,反应二的速率增大
D.对反应二,在180—200℃,温度越高,Ni(CO)4(g)的转化率越高
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
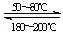 Ni(CO)4(g) 该反应的△H
Ni(CO)4(g) 该反应的△H| cCO23 |
| cCO3 |
| cCO23 |
| cCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
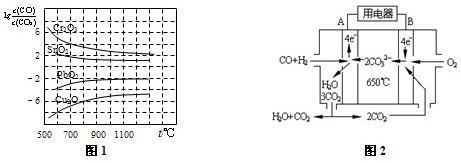
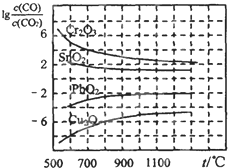 一氧化碳是一种用途相当广泛的化工基础原料.
一氧化碳是一种用途相当广泛的化工基础原料.| 50~80℃ |
| 180~200℃ |
| c(CO) |
| c(CO2) |
| c3(CO2) |
| c3(CO) |
| c3(CO2) |
| c3(CO) |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
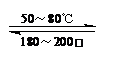 Ni(CO)4(g) 该反应的△H
Ni(CO)4(g) 该反应的△H
| 10 |
| 11 |
| ||
| 氢离子 |
| 石灰水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 50~80℃ |
| 180~200℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 50-80℃ |
| 180-200℃ |
| A、50~80℃时,适当增大压强,有利于Ni(CO)4的生成 | ||
| B、利用上述原理提纯粗镍需要消耗大量的CO气体 | ||
| C、50~200℃范围内,该反应的平衡常数随温度的升高而减小 | ||
D、该反应的平衡常数表达式是K=
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com