
| W | X | Y | Z | |
| 结构 或性质 | 最高价氧化物对应的水 化物与其气态氢化物反 应得到离子化合物 | 焰色反应呈黄色 | 在同周期主族元素形成的简单离子中,离子半径最小 | 最高正价与最 低负价之和为6 |
 .
.分析 四种短周期元素W、X、Y、Z的原子序数依次增大,W最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物,则W为N元素;X元素焰色反应呈黄色,则X为Na;在同周期主族元素形成的简单离子中,Y离子半径最小,原子序数大于Na,则Y为Al;Z的最高正价与最低负价之和为6,则Z为Cl元素,据此解答.
解答 解:四种短周期元素W、X、Y、Z的原子序数依次增大,W最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物,则W为N元素;X元素焰色反应呈黄色,则X为Na;在同周期主族元素形成的简单离子中,Y离子半径最小,原子序数大于Na,则Y为Al;Z的最高正价与最低负价之和为6,则Z为Cl元素.
(1)N元素和氢可形成离子化合物为NH4H,其电子式为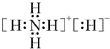 ,
,
故答案为: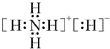 ;
;
(2)Y元素和Z元素可形成AlCl3化合物,可用于净水剂,净水原理:Al3++3H2O=Al(OH)3(胶体)+3H+,
故答案为:Al3++3H2O=Al(OH)3(胶体)+3H+;
(3)①a.NaOH属于强碱,氢氧化铝能与氢氧化钠反应生成偏铝酸钠与水,氢氧化铝表现酸性,则说明Na的金属性比Al强,故a正确;
b.硫酸钠溶液呈中性,硫酸铝溶液应铝离子水解呈酸性,说明氢氧化钠碱性比氢氧化铝的强,则说明Na的金属性比Al强,故b正确;
c.金属性越强,单质与水反应越容易,故c正确;
d.金属性强弱与失去电子难易程度有关,与失去电子数目多少无关,故d错误,
故选:abc;
②由Na、Al、氢、氧四种元素所组成的化合物,能与盐酸以1:4反应生成两种常见盐和水,则该化合物的化学式为:NaAl(OH)4,
故答案为:NaAl(OH)4;
(4)W(氮元素)的一种氢化物HN3可用于有机合成,其酸性与醋酸相似.体积和浓度均相等的HN3与NaOH混合得到NaN3溶液,溶液中N3-离子水解而成碱性,故混合后溶液中离子浓度由大到小的顺序是:c(Na+)>c(N3-)>c(OH-)>c(H+),
故答案为:c(Na+)>c(N3-)>c(OH-)>c(H+).
点评 本题考查结构性质位置关系、盐类水解、元素化合物性质等,难度中等,推断元素是解题关键,注意理解掌握金属性强弱比较,(4)注意利用信息确定HN3为弱酸.


科目:高中化学 来源: 题型:填空题
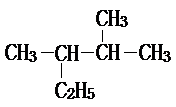 2,3-二甲基戊烷
2,3-二甲基戊烷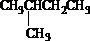
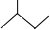
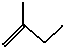 C5H10.
C5H10.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
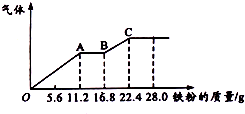 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体),向另一份中逐渐加入铁粉,产生气体的最随铁粉质量增加的变化如图所示,下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体),向另一份中逐渐加入铁粉,产生气体的最随铁粉质量增加的变化如图所示,下列分析或结果错误的是( )| A. | H2SO4浓度为5mol•L-1 | |
| B. | 第二份溶液中最终溶质为FeSO4 | |
| C. | 每份混合酸中NO3-物质的量为0.2mol | |
| D. | OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
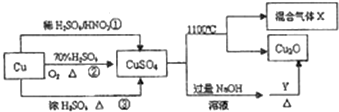
| A. | 相对于途径①、③,途径②更好地体现了绿色化学思想 | |
| B. | Y可以是葡萄糖溶液 | |
| C. | CuSO4在1100℃所得混合气体X中一定有O2 | |
| D. | 途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
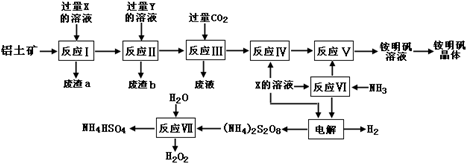
| SO2Cl2 | Cl2 | SO2 | |
| 熔点/℃ | -54.1 | -101 | -72.4 |
| 沸点/℃ | 69.1 | -34.6 | -10 |
| 性质 | 遇水发生 剧烈水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8个中子的碳原子:${\;}_{6}^{12}$C | B. | HClO的结构式:H-Cl-O | ||
| C. | N2H4的电子式: | D. | 甲酸的分子式:CH2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸铅蓄电池的负极:Pb-2e-═Pb2+ | |
| B. | 锌银纽扣电池的正极:Ag2O+2e-+H2O═2AgOH | |
| C. | 碱性锌锰电池的负极:Zn-2e-+2OH-═Zn(OH)2 | |
| D. | 氢氧碱性燃料电池的正极:2H2O+4e-═O2+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水 | B. | 浓盐酸 | C. | 高锰酸钾溶液 | D. | 苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com