
| A、醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(HCOO-) |
| B、0.01mol/L的HCOOH溶液中加水稀释,溶液中c(OH-)减小 |
| C、HCOOH溶液中加少量的HCOONa固体,平衡逆向移动 |
| D、常温下pH=2的HCOOH溶液与pH=12的NaOH溶液等体积混合后,pH<7 |


科目:高中化学 来源: 题型:
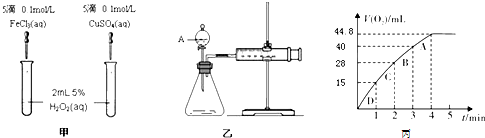
查看答案和解析>>
科目:高中化学 来源: 题型:
| 高温、高压 |
| 催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| O2 |
| 点燃 |
| H2SO4 |
| NaOH |
| HCl |
| HCl(aq) |
| △ |
| O2 |
| 点燃 |
| H2O |
| H2O |
| O2 |
| A、①⑤ | B、②⑤ | C、③④ | D、②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该物质一定是钾的化合物 |
| B、该物质中一定含有钾元素 |
| C、不能确定该物质是否含有钾元素 |
| D、该物质一定是金属钾 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、对该反应体系加热 |
| B、滴加几滴浓硫酸 |
| C、加入少量氯化钠溶液 |
| D、不用铁片,改用铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、液态HCl和固体NaCl均不导电,但HCl、NaCl均是电解质 |
| B、NH3、CO2的水溶液均导电,所以NH3、CO2均是电解质 |
| C、铜、石墨均导电,但他们都不是电解质,而是非电解质 |
| D、酸碱盐和氧化物都是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| A、0.4Q1+0.05Q2 |
| B、0.4Q1+0.1Q2 |
| C、0.4Q1+0.05Q3 |
| D、0.4Q1+0.1Q3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com