
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,常用于水的消毒以及纺织高漂白。过氧化氢法生产亚氯酸钠的流程图如下
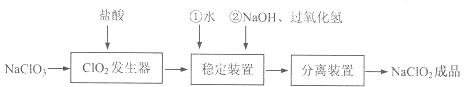
已知NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O且NaClO2在碱性条件下稳定性较高。试回答下列问题:
(1)在ClO2发生器中同时有氯气产生,则在发生器中发生反应的化学方程式为
(2)在NaClO2稳定装置中,H2O2作 (选填序号)。
A.氧化剂 B.还原剂
C.既作氧化剂又作还原剂 D.既不作氧化剂也不作还原剂
(3)在实验室模拟“固体分离装置”中的技术,必须进行的实验操作是 (按实验后顺序填写操作代号)。
A.过滤 B.加热 C.分液 D.蒸馏 E.冷却
(4)经查阅资料知道:当pH≤2.0时,ClO-2能被I完全还原成Cl—;
溶液中Na2S2O3能与I2反应生成NaI和Na2S4O6。
欲测定成品中NaClO2的含量,现进行如下操作:

①步骤Ⅱ中发生反应的离子方程式是 ,
步骤Ⅲ中达到滴定终点时的现象是 。
②若上述滴定操作中用去了V mL Na2S2O3溶液,则样品中NaClO2的质量分数 (用字母表示)。
【知识点】工艺流程题 A4 B1 D2 C1 J1 B2
【答案解析】(1)2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
(2)B (3)BEA
(4)ClO2-+4H++4I-=2I2+Cl-+2H2O
滴入最后一滴标准液(Na2S2O3溶液),溶液由蓝色变为无色,且半分钟内不变色
9.05×10-2VC/4W
解析: ⑴ClO2发生器中有氯气产生,是NaClO2氧化浓盐酸:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
⑵ClO2在稳定装置中变为NaClO2,发生的是还原反应,因此H2O2作还原剂
⑶根据NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2·3H2O知采取冷却结晶的方法,即加热→冷却→过滤。
⑷①根据当pH≤2.0时,ClO-2能被I完全还原成Cl—知步骤Ⅱ中发生反应是ClO2-将I-氧化为I2,步骤Ⅲ发生的反应是2Na2S2O3+I2=2NaI+Na2S4O6,即终点时的现象是滴入最后一滴标准液(Na2S2O3溶液),溶液由蓝色变为无色,且半分钟内不变色
②NaClO2~2I2~4 Na2S2O3
90.5 4mol
m VC×10-3,m=9.05×10-2VC/4,因此质量分数为9.05×10-2VC/4W
【思路点拨】多步反应计算采取关系式法;根据物质的溶解度随温度的变化结晶方法有蒸发结晶(物质的溶解度随温度的变化小)和冷却结晶(物质的溶解度随温度的变化大)。


科目:高中化学 来源: 题型:
利用从冬青中提取的有机物A合成抗结肠炎药物Y及其他化学品,合成路线如下:
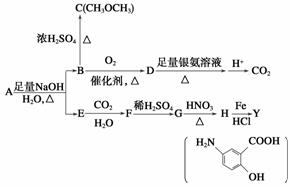
提示: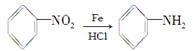
根据上述信息回答:
(1)D不与NaHCO3溶液反应,D中官能团的名称是________,B→C的反应类型是________________________________________________________________________。
(2)写出A生成B和E的化学反应方程式
________________________________________________________________________
________________________________________________________________________。
(3)A的同分异构体I和J是重要的医药中间体,在浓硫酸的作用下,I和J分别生成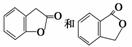 ,鉴别I和J的试剂为________________。
,鉴别I和J的试剂为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是某研究小组采用电解法处理石油炼制过程中产生的大量H2S废气的工艺流程。该方法对H2S的吸收率达99%以上,并可制取H2和S。下列说法正确的是( )
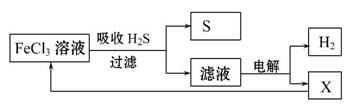
A.吸收H2S的离子方程式为Fe3++H2S====Fe2++S↓+2H+
B.电解过程中的阳极反应主要为2Cl--2e-====Cl2↑
C.该工艺流程体现绿色化学思想
D.实验室可用点燃充分燃烧的方法消除H2S污染
查看答案和解析>>
科目:高中化学 来源: 题型:
氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如图所示步骤进行操作。
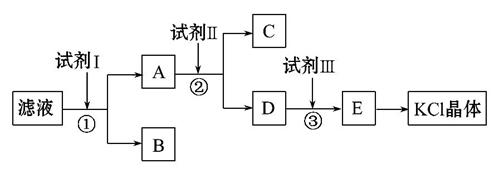
回答下列问题:
(1)起始滤液的pH__________7(填“大于”“小于”或“等于”),其原因是______________________________________________;
(2)试剂Ⅰ的化学式为______________,①中发生反应的离子方程式为______
__________________________________________________________________;
(3)试剂Ⅱ的化学式为______________,②中加入试剂Ⅱ的目的是__________
__________________________________________________________________;
(4)试剂Ⅲ的名称是__________,③中发生反应的离子方程式为___________
__________________________________________________________________;
(5)某同学称取提纯的产品0.775 9 g,溶解后定容在100 mL容量瓶中,每次取25.00 mL溶液,用0.100 0 mol·L-1的硝酸银标准溶液滴定,三次滴定消耗标准溶液的平均体积为25.62 mL,该产品的纯度为________(列式并计算结果)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子反应方程式正确的是( )
A.在硫酸铝溶液中加入过量氨水:Al3+ + 4OH- = AlO2-+2H2O
B.碳酸氢镁溶液中加入过量石灰水:
Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+MgCO3↓
C.往FeCl3溶液中加入Fe粉:2Fe3+ +Fe =3Fe2+
D.氧化亚铁溶于稀硝酸:FeO+2H+=Fe2++H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
在水溶液中能大量共存的一组是
A.Ba2+、Na+、SO42—、Cl— B.MnO4—、SO32—、H+、K+
C.AlO2—、Mg2+、K+ 、HCO3— D.K+、 Na+、 NO3— 、SO42—
查看答案和解析>>
科目:高中化学 来源: 题型:
.常温下,pH=1的某溶液A中含有NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、NO3-、Cl-、I-、SO42-中的4种,且各离子的物质的量浓度均为0.1mol/L,现取该溶液进行有关实验,实验结果如下图所示:
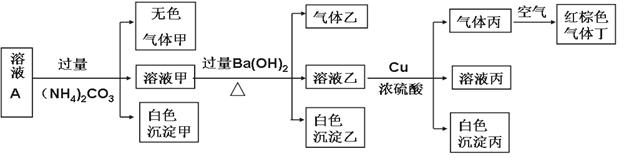
下列有关说法正确的是 ( )
A. 沉淀乙一定有BaCO3,可能有BaSO4
B.实验消耗Cu 14.4g,则生成气体丁的体积为3.36L
C.该溶液中一定有NO3-、Al3+、SO42-、Cl-四种离子
D.生成的甲、乙、丙气体均为无色的易溶于水气体
查看答案和解析>>
科目:高中化学 来源: 题型:
当1 mol某气态烃与2 mol Cl2发生加成反应时,分子中的不饱和碳原子全部转化为饱和碳原子,所得产物再与2 mol Cl2进行取代反应后,生成只含C、Cl两种元素的化合物。则该气态烃是( )
A.乙烯 B.乙炔 C.丙烯 D.丙炔
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com