
【题目】已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是( )
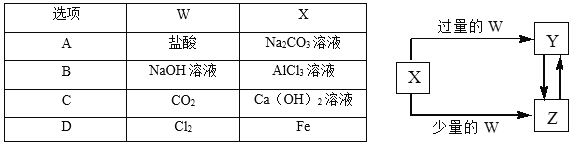
A. AB. BC. CD. D
【答案】D
【解析】
A.X为Na2CO3,W为盐酸时,碳酸钠和少量盐酸反应生成Z(碳酸氢钠),碳酸钠和过量盐酸反应生成Y(二氧化碳),Z(碳酸氢钠)加入盐酸可以生成Y(二氧化碳),Y(二氧化碳)通入氢氧化钠溶液中可以生成Z(碳酸氢钠),符合转化关系,故不选A;
B.X为AlCl3,W为NaOH时,氢氧化钠过量生成Y(偏铝酸钠),氢氧化钠少量生成Z(氢氧化铝),Z(氢氧化铝)加入氢氧化钠生成Y(偏铝酸钠),Y(偏铝酸钠)加入弱酸生成Y(偏铝酸钠),符合转化关系,故不选B;
C..X为Ca(OH)2,W为CO2,二氧化碳过量生成 Y(Ca(HCO3)2)、二氧化碳少量生成Z(CaCO3),Y(Ca(HCO3)2)与Ca(OH)2反应可生成Z(CaCO3),Z(CaCO3)与CO2、水反应可生成Y(Ca(HCO3)2),符合转化关系,故不选C;
D.不论Cl2过量与不足,与金属Fe反应的产物均为FeCl3,因此不能形成题中所示的回路;
答案:D。


科目:高中化学 来源: 题型:
【题目】光刻胶是大规模集成电路印刷电路板技术中的关键材料,某一光刻胶的主要成分如图所示,下列有关说法正确的是( )

A. 该物质可经过缩聚反应制得
B. 1 mol该物质可消耗4 mol H2
C. 该物质可稳定存在于碱性溶液中
D. 合成此高聚物的单体的化学式为C11H10O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁、铜合金加入到稀硝酸中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3mol·L-1 的NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述中正确的是
A. 开始加入合金的质量可能为16.4g
B. 标准状况下产物NO的体积为22.4L
C. 生成沉淀完全时消耗NaOH溶液的体积为100mL
D. 参加反应的硝酸的物质的量为0.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是几种常见的加热装置。

请回答下列问题:
(1)A、B、C、D四种装置都是用酒精灯直接加热,E、F装置加热时需垫上________。其中F装置中对试管的加热方式是_____________________________,使用这种加热方式的目的是______________________。
(2)用H2还原CuO可选用____________(填字母,下同)装置。
(3)加热NH4Cl与Ca(OH)2的固体混合物制NH3可选用___________装置。
(4)胆矾中结晶水含量的测定可选用_______装置。
(5)乙酸乙酯的制备可选用____________装置。
(6)MnO2与浓盐酸混合制Cl2可选用_____装置。若该装置只加热液体时,受热容器内必须放____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质间可能包括多步反应,其总的离子方程式正确的是 ( )
A. 向NaClO溶液中通入过量SO2:ClO-+SO2+H2O===HClO+HSO3-
B. 向FeBr2溶液中通入少量Cl2:2Fe2++4Br-+3Cl2===2Fe3++2Br2+6Cl-
C. 向 AlCl3溶液中投入过量Na:Al3++4Na+2H2O===AlO2-+4Na++2H2↑
D. 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42- 沉淀完全:2Al3++3SO![]() +3Ba2++6OH-===2Al(OH)3↓+3BaSO4↓
+3Ba2++6OH-===2Al(OH)3↓+3BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学键的叙述,正确的是( )
A. 非金属元素原子之间形成的一定是共价键
B. 离子化合物中一定含有离子键
C. 单质分子中一定存在化学键
D. 含有共价键的化合物一定是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】俄罗斯科学家用含20个质子的钙的一种原子轰击含95个质子的镅原子,结果4次成功合成4个第115号元素的原子。这4个原子生成数微秒后衰变成第113号元素。下列有关叙述正确的是
A. 115号元素在第六周期
B. 113号元素在第七周期ⅢA族
C. 115号和113号元素都是非金属元素
D. 镅元素和115号元素不在同一周期
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】计算后填空:
(1)在标准状况下,448 mL某气体的质量为0.64 g,这种气体的相对分子质量为________。
(2)某氯化铁与氯化钠的混合液,已知c(Fe3+)=0.2 mol·L-1,c(Cl-)=1 mol·L-1。则c(Na+)为________。
(3)19 g某二价金属的氯化物RCl2中含有0.4 mol的Cl-,则R的相对原子质量为__________。
(4)500mL Fe2(SO4)3溶液中含Fe3+ 28 g,则溶液中SO42-的物质的量浓度为________mol·L-1。
(5)在无土栽培中,配制1 L含5 mol NH4Cl、1.6 mol KCl、2.4 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需KCl、NH4Cl的物质的量分别为________、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用3g块状大理石与30mL3mol/L盐酸反应制取CO2气体,若要增大反应速率,可采取的措施是( )
①再加入30mL1mol/L盐酸 ②改用30mL6mol/L盐酸 ③改用3g粉末状大理石 ④适当升高温度
A. ①②④ B. ②③④ C. ①③④ D. ①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com