
| A. | H20分子中只含有非极性共价键 | |
| B. | H20分子中只含有极性共价键 | |
| C. | 水分子间只存在氢键 | |
| D. | 冷却反应堆用水在地球上常温下是固态 |
分析 水分子中H原子与氧原子之间形成1对共用电子对,由于O元素电负性很大,共用电子对偏向O原子,偏离H原子,共价键为极性键,使的H原子近似裸露的质子,水分子之间形成氢键,冷却反应堆用水在地球上常温下应是液态,通过水循环带走热量使反应堆降温.
解答 解:A.水分子中H原子与氧原子之间形成1对共用电子对,由于O元素电负性很大,共用电子对偏向O原子,偏离H原子,共价键为极性键,故A错误;
B.水分子中共价键为极性键,故B正确;
C.O原子电负性很强,共用电子对偏向O原子,偏离H原子,使的H原子近似裸露的质子,水分子之间形成氢键,水分子之间还存在范德华力,故C错误;
D.冷却反应堆用水在地球上常温下应是液态,通过水循环带走热量使反应堆降温,故D错误,
故选:B.
点评 本题以福岛核反应堆事故为载体,考查共价键、氢键等,注意掌握共价键形成条件与分类,理解掌握氢键的形成,注意氢键对物质性质的影响.


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.8molCH4 | B. | 66gCO2 | ||
| C. | 标准状况下44.8L的O2 | D. | NA个水分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  根据图可判断可逆反应A2(g)+3B2(g)?2AB3(g),正反应是吸热反应 | |
| B. | 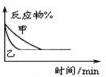 如图表示压强对反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 | |
| C. | 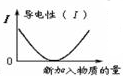 图可表示乙酸溶液中通入氨气至过量的过程中溶液导电性的变化 | |
| D. | 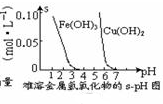 根据图可知,若除去CuSO4溶液中的Fe3+,可向溶液中加入CuO,调节pH在4~5之间即可 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
浓度/mol•L-1 时间/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
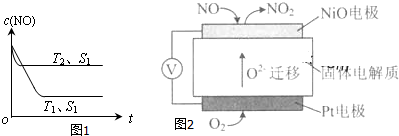
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
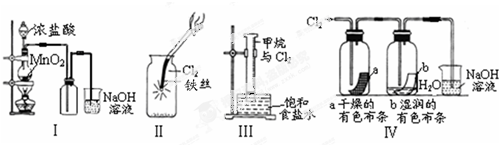
| A. | Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗完 | |
| B. | Ⅱ图中:有棕黄色的雾生成 | |
| C. | Ⅲ图中:量筒中发生了加成反应 | |
| D. | Ⅳ图中湿润的有色布条能褪色,将浓硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com