
【题目】醋酸亚铬水合物[Cr(CH3COO)2]2·2H2O(相对分子质量为376)是一种氧气吸收剂,为红棕色晶体,潮湿时易被氧化,微溶于乙醇,不溶于水和乙醚(易挥发的有机溶剂)。其制备装置及步骤如下:
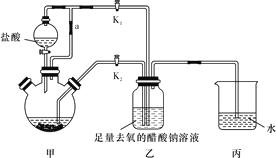
①待三颈烧瓶内的溶液由深绿色(Cr3+)变为亮蓝色(Cr2+)时,将溶液转移至装置乙中,当出现大量红棕色晶体时,关闭分液漏斗的旋塞。
②将装置乙中混合物快速过滤、洗涤和干燥,称量得到 [Cr(CH3COO)2]2·2H2O。
③检查装置气密性后,往三颈烧瓶中依次加入过量锌粒、适量CrCl3溶液。
④关闭K2,打开K1,旋开分液漏斗的旋塞并控制好滴速。
(1)正确的实验步骤为:_________________。
(2)装置甲中连通管a的作用是_______________________________________。
(3)三颈烧瓶中的Zn除了与盐酸生成H2外,发生的另一个反应的离子方程式为_______________________________________________。
(4)实现步骤①中溶液自动转移至装置乙中的实验操作为_______________________。
(5)步骤④目的是___________________________________________。
(6)洗涤产品时,依次用去氧的冷蒸馏水、无水乙醇、乙醚,目的是_________________。
(7)已知其它反应物足量,实验时取用的CrCl3溶液中含溶质9.51g,实验后得干燥纯净的[Cr(CH3COO)2]2·2H2O 9.48g,则该实验所得产品的产率为____(不考虑溶解的醋酸亚铬水合物)(用百分数表示,保留3位有效数字)。
【答案】③④①② 平衡气压,使分液漏斗中的盐酸顺利流下 2Cr3++Zn===2Cr2++Zn2+ 关闭K1,打开K2 让Zn与盐酸反应生成的H2排尽装置内的空气,防止产品被氧化 为了去除可溶性杂质和水分 84.0%
【解析】
(1) 装置甲:分液漏斗盛装稀盐酸,在圆底烧瓶中和锌反应Zn+2HCl═ZnCl2+H2↑,同时发生2CrCl3+Zn═2CrCl2+ZnCl2,生成氢气,用来增大压强把生成的CrCl2溶液压入装置乙中;装置乙:2Cr2++4CH3COO-+2H2O═[Cr(CH3COO)2]22H2O↓,装置丙是保持装置压强平衡,同时避免空气进入,故正确的实验步骤为:③④①②;
(2)装置甲中连通管a的作用是平衡气压,使分液漏斗中的盐酸顺利流下;
(3)装置甲:分液漏斗盛装稀盐酸,在圆底烧瓶中和锌反应Zn+2HCl═ZnCl2+H2↑,同时发生2CrCl3+Zn═2CrCl2+ZnCl2,,该反应的离子反应为:2Cr3++Zn===2Cr2++Zn2+;
(4)实验开始生成H2气后,为使生成的CrCl2溶液与CH3COONa溶液顺利混合,打开K2关闭K1,把生成的CrCl2溶液压入装置乙中反应,故答案为:关闭k1,打开k2;
(5)步骤④目的是让Zn与盐酸反应生成的H2排尽装置内的空气,防止产品被氧化;
(6)醋酸亚铬水合物不溶于冷水和醚,微溶于醇,易溶于盐酸,所以可以选用冷水、无水乙醇和乙醚洗涤[Cr(CH3COO)2]2·2H2O产品,洗涤产品时,依次用去氧的冷蒸馏水、无水乙醇、乙醚,目的是为了去除可溶性杂质和水分;
(7)CrCl3为![]() =0.06mol,得到CrCl2为0.06mol,而CH3COONa为1.5mol,由方程式可知CH3COONa足量,则理论上可以得到[Cr(CH3COO)2]22H2O的质量为0.06mol×
=0.06mol,得到CrCl2为0.06mol,而CH3COONa为1.5mol,由方程式可知CH3COONa足量,则理论上可以得到[Cr(CH3COO)2]22H2O的质量为0.06mol×![]() ×376g/mol=11.28g,所得产品的产率为
×376g/mol=11.28g,所得产品的产率为 ![]() ×100%=84.0%。
×100%=84.0%。


科目:高中化学 来源: 题型:
【题目】氮气氢气合成氨过程中制氢气的原理如下:
①CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH=+206.4 kJ·mol-1
CO(g)+3H2(g) ΔH=+206.4 kJ·mol-1
②CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
(1)对于反应①,一定可以提高平衡体系中H2的百分含量,又能加快反应速率的措施是_______。
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
(2)利用反应②,将CO进一步转化,可提高H2的产量。若1 mol CO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18 mol CO、CO2和H2的混合气体,则CO的转化率为________。
(3)图(a)表示500 ℃、60.0 MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:____________。
(4)依据温度对合成氨反应的影响,在图(b)坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图________。


查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化钛(TiCl4)是制取航天航空工业材料——钛合金的重要原料。由钛铁矿(主要成分是FeTiO3)制备TiCl4,同时获得副产品甲的工业生产流程如下:
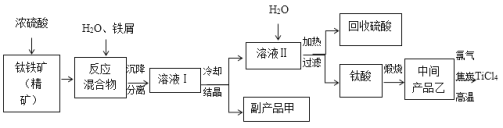
(1)已知酸浸反应FeTiO3+2H2SO4===FeSO4+TiOSO4+2H2O,则FeTiO3中铁元素的化合价为___________。
(2)上述生产流程中加入铁屑的目的是使Fe3+还原为Fe2+,且反应得到的溶液中含钛元素的离子只有TiO2+,该过程发生的主要反应有:
①2Fe3++Fe===3Fe2+ ; ②2TiO2++Fe+4H+===2Ti3++Fe2++2H2O;③______________________________________。
(3)加热TiOSO4溶液可制备TiO2·nH2O胶体,其反应的化学方程式为__________________。
(4)由TiO2·nH2O胶体制得固体TiO2·nH2O,再用酸清洗除去其中的Fe(OH)3杂质,还可制得钛白粉。已知25℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+![]() Fe3++3H2O的平衡常数K=___________________。
Fe3++3H2O的平衡常数K=___________________。
(5)可循环利用的物质是_________,副产品甲含结晶水,其化学式是_______________。
(6)依据下表信息,要精制含少量SiCl4杂质的TiCl4,可采用___________方法。
TiCl4 | SiCl4 | |
熔点/℃ | -25.0 | -68.8 |
沸点/℃ | 136.4 | 57.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】放热反应CO(g)+H2O(g)![]() CO2(g)+H2(g)在温度t1时达到平衡,c1(CO)=c1(H2O)=1.0 mol·L-1,其平衡常数为K1。升高反应体系的温度至t2时,反应物的平衡浓度分别为c2(CO)和c2(H2O),平衡常数为K2,则( )
CO2(g)+H2(g)在温度t1时达到平衡,c1(CO)=c1(H2O)=1.0 mol·L-1,其平衡常数为K1。升高反应体系的温度至t2时,反应物的平衡浓度分别为c2(CO)和c2(H2O),平衡常数为K2,则( )
A. K2和K1的单位均为mol·L-1
B. K2>K1
C. c2(CO)=c2(H2O)
D. c1(CO)>c2(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是CO和水蒸气发生反应生成CO2和H2的途径和三个状态的能量,该反应为吸热反应,试问:
E1:CO+H2O![]() E2:C+2H+2O
E2:C+2H+2O![]() E3:CO2+H2
E3:CO2+H2
(1)步骤1、2分别是吸热过程还是放热过程?
步骤1:______,步骤2:______。
(2)比较E1、E3的大小______。
(3)已知,25℃时,C(石墨)+1/2O2(g) ═ CO(g) ΔH1=-111 kJ/mol;
H2(g)+1/2O2(g) ═ H2O(g) ΔH2=-242 kJ/mol;
C(石墨)+O2(g) ═ CO2(g) ΔH3=-394 kJ/mol。
则CO和H2O(g)反应的热化学方程式为:______。
(4)含1 mol Ba(OH)2的稀溶液与足量稀盐酸反应放出114.6 kJ的热量,写出该反应中和热的热化学方程式:______。
(5)在C2H2(g)完全燃烧生成CO2和液态水的反应中,每转移5NA个电子放出a kJ的热量。则表示C2H2的燃烧热的热化学方程式为:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠晶体(Na2S2O3·5H2O,M=248 g·mol1)可用作定影剂、还原剂。回答下列问题:
(1)已知:Ksp(BaSO4)=1.1×1010,Ksp(BaS2O3)=4.1×105。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:
试剂:稀盐酸、稀H2SO4、BaCl2溶液、Na2CO3溶液、H2O2溶液
实验步骤 | 现象 |
①取少量样品,加入除氧蒸馏水 | ②固体完全溶解得无色澄清溶液 |
③___________ | ④___________,有刺激性气体产生 |
⑤静置,___________ | ⑥___________ |
(2)利用K2Cr2O7标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
①溶液配制:称取1.2000 g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在__________中溶解,完全溶解后,全部转移至100 mL的_________中,加蒸馏水至____________。
②滴定:取0.00950 mol·L1的K2Cr2O7标准溶液20.00 mL,硫酸酸化后加入过量KI,发生反应: Cr2O72+6I+14H+![]() 3I2+2Cr3++7H2O。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O32
3I2+2Cr3++7H2O。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O32![]() S4O62+2I。加入淀粉溶液作为指示剂,继续滴定,当溶液__________,即为终点。平行滴定3次,样品溶液的平均用量为24.80 mL,则样品纯度为_________%(保留1位小数)。
S4O62+2I。加入淀粉溶液作为指示剂,继续滴定,当溶液__________,即为终点。平行滴定3次,样品溶液的平均用量为24.80 mL,则样品纯度为_________%(保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数,下列说法正确的是
A. 162g淀粉和纤维素混合物中氧原子的数目为5NA
B. 常温时,pH=5的盐酸中水电离的OH-数目为10-9NA
C. 5mol的CH3COONa固体溶于水所得溶液中CH3COO-数目为5NA
D. 22.4L Cl2与足量的铁反应,转移的电子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.下列叙述中不正确的是( )
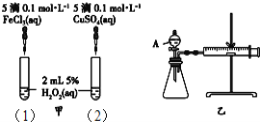
A. 实验中H2O2分解的速率为(1)>(2)
B. 图乙实验可通过测定相同状况下,产生的气体体积与反应时间来比较反应速率
C. H2O2分解的热化学方程式2H2O2(l)═2H2O(l)+O2(g)△H>0
D. 图甲中(1)、(2)两个实验中H2O2分解的△H相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图![]() 为直流电源,
为直流电源,![]() 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸,![]() 为电镀槽.接通电路后发现
为电镀槽.接通电路后发现![]() 上的c点显红色,为实现铁上镀锌,接通
上的c点显红色,为实现铁上镀锌,接通![]() 后,使c、d两点短路.下列叙述正确的是
后,使c、d两点短路.下列叙述正确的是
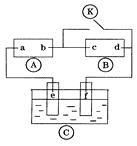
A. a为直流电源的负极
B. c极发生的反应为2H++2e-=H2↑
C. f电极为锌板
D. e极发生还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com