
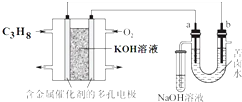
 �ü��Ա���ȼ�ϵ�ص���±ˮ����Cl-��Br-��Na+��Mg2+����װ����ͼ��ʾ��a��bΪʯī�缫��������˵����ȷ���ǣ�������
�ü��Ա���ȼ�ϵ�ص���±ˮ����Cl-��Br-��Na+��Mg2+����װ����ͼ��ʾ��a��bΪʯī�缫��������˵����ȷ���ǣ�������| A�� | ��ع���ʱ��������ӦʽΪ��C3H8+26OH--20e-�T3CO${\;}_{3}^{2-}$+17H2O | |
| B�� | ���ʱ��a�缫��Χ���ȷŵ����Br-������Cl-��˵��������������ͬʱǰ�ߵĻ�ԭ��ǿ�ں��� | |
| C�� | ���ʱ������������·���ǣ����������·����������Һ������������ | |
| D�� | ����������ģ������������ 0.16 g O2ʱ��a����Χ�����0.71 g Cl2 |
���� ������Է��Ľ���������ԭ��Ӧ��Ϊԭ��أ�ȼ��C3H8ͨ�븺����ʧ���ӷ���������Ӧ��ͨ�������ĵ缫���������õ����ӷ�����ԭ��Ӧ���ұ��ǵ��أ����Դ������������a�����������Դ������������b�������������������ӷŵ磬�����������ӷŵ磬���ӴӸ������������������������������ݴ˽��
��� �⣺������Է��Ľ���������ԭ��Ӧ��Ϊԭ��أ�ȼ��C3H8ͨ�븺����ʧ���ӷ���������Ӧ��ͨ�������ĵ缫���������õ����ӷ�����ԭ��Ӧ���ұ��ǵ��أ����Դ������������a�����������Դ������������b�������������������ӷŵ磬�����������ӷŵ磬���ӴӸ�����������������������������
A�����Խ����У�ȼ��C3H8�ڸ�����ʧ���ӷ���������Ӧ���缫��ӦʽΪC3H8+26OH--20e-�T3CO32-+17H2O����A��ȷ��
B����ԭ��ǿ�������������ȷŵ磬���ʱ��a�缫��Χ���ȷŵ����Br-������Cl-�����Ի�ԭ�ԣ�Br-��Cl-����B��ȷ��
C�����ʱ����������·���ǣ����������·�����������������·�����������Ӳ�������Һ����������C����
D������ת�Ƶ������֪�������������0.16gO2ʱ��ת�Ƶ���0.02mol��a���缫��ӦʽΪ2Br--2e-=Br2����ת��0.02mol����������0.01mol����D����
��ѡAB��
���� ���⿼����ԭ��غ͵��أ���ȷԭ��غ͵���ԭ���ǽⱾ��ؼ���֪�����ӵķŵ�˳���״�ѡ����C��ע����Ӳ�����������Һ����Һ���������Ӷ����ƶ����γɵ������ѶȲ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �ۢܢ� | C�� | �ۢ� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al��OH��3 | B�� | NaCl��Һ | C�� | K2SO4��Һ | D�� | ϡH2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ø�̵�����˹��̵�����Ч���������º� | |
| B�� | ���۲���ɫ�������ֻƽ���ͭп�Ͻ� | |
| C�� | �����õع������Ƶ����ﺽ���ؿ��ɣ���־���ҹ�����ҵ�ڽ��ܼ������������ҵ���н� | |
| D�� | ��Һȼ�ϵ�ص�ԭ���������������½���Һ�е��л���ת��Ϊ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢ� | B�� | �٢ۢݢ� | C�� | �٢ۢܢ� | D�� | �٢ۢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ���� | HA�����ʵ���Ũ�ȣ�mol•L-1�� | NaOH�����ʵ���Ũ�ȣ�mol•L-1�� | ��Ϻ���Һ��pH |
| �� | 0.1 | 0.1 | pH=a |
| �� | 0.12 | 0.1 | pH=7 |
| �� | 0.2 | 0.1 | pH��7 |
| �� | 0.1 | 0.1 | pH=10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ����4�������ţ���ԭ�ӡ��������ǻ����Ȼ� | |
| B�� | �����Ȼ������봼�����ʷ���������Ӧ | |
| C�� | ���з��ǻ�����������NaHCO3��Һ��Ӧ����CO2 | |
| D�� | ������ԭ�ӣ����������ƴ���Һ�м��ȣ��ɷ�����ȥ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ϩ�̶����۷е㣬�������ϩͨ���Ӿ۷�Ӧ�ϳ� | |
| B�� | �л��������࣬�����к���̼����Ԫ�ص����ʼ�Ϊ�л��� | |
| C�� | ʯ�͵ķ����ú�ĸ�������������仯 | |
| D�� | �������е��л����ж�����һ�ֻ���ֹ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
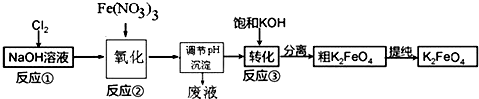

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com