
| A. | 气态氢化物的热稳定性:Y>Z | |
| B. | W与另外三种元素均可形成离子键 | |
| C. | 简单离子半径:W>Y>Z | |
| D. | W和Y可形成阴阳离子个数比是1:1的化合物 |
分析 X、Y、Z、W四种短周期元素,化合物XZ可刻蚀玻璃,XZ为HF,X为H,Z为F;Y元素原子的最外层电子数是内层电子数的3倍,Y为O元素;W+与Z的简单离子有相同的电子层排布,可知W为Na,然后结合元素周期律及元素化合物知识来解答.
解答 解:由上述分析可知,X为H,Y为O,Z为F,W为Na,
A.非金属性F>O,则气态氢化物的热稳定性:Y<Z,故A错误;
B.NaH、Na2O、NaF均含离子键,故B正确;
C.具有相同电子层结构的离子中原子序数大的离子半径小,则简单离子半径:Y>Z>W,故C错误;
D.W和Y可形成Na2O或Na2O2,阴阳离子个数比是1:2,故D错误;
故选B.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构、元素化合物知识来推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ①②④ | C. | ①②③④ | D. | ①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
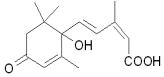 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )| A. | 含有碳碳双键、羟基、羰基、苯环、羧基 | |
| B. | 该有机物的分子式为C15H20O4 | |
| C. | 分子中所有的原子有可能在同一平面 | |
| D. | 该有机物属于芳香族化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | 过量二氧化硫通入氢氧化钠溶液中:SO2+OH-═SO32-+H2O | |
| D. | 氯化铁溶液与铜粉反应:Cu+2Fe3+═2Fe2++Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | |
| Z | W |
| A. | 简单离子半径:W>Z>Y | |
| B. | 气态氢化物的稳定性:Y>Z>W | |
| C. | 最常见气态氢化物的沸点:Y>X>Z | |
| D. | 最高价氧化物对应的水化物酸性:Z>W |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
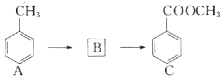 化合物C是某合成路线的中间体,可通过下列(如图)路径合成:
化合物C是某合成路线的中间体,可通过下列(如图)路径合成: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑥ | B. | ①③④⑥ | C. | ③④⑤⑥ | D. | ①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com