
| A. | 30 g•mol-1或46 g•mol-1 | B. | 44 g•mol-1或80 g•mol-1 | ||
| C. | 28 g•mol-1 | D. | 46 g•mol-1 |
分析 0.96g Mg的物质的量为$\frac{0.96g}{24g/mol}$=0.04mol,6.3g HNO3的物质的量为$\frac{6.3g}{63g/mol}$=0.1mol,反应生成Mg(NO3)2为0.04mol,假设0.1mol-0.04mol×2=0.02mol的HNO3全部其氧化剂作用,根据电子转移守恒计算N元素在还原产物中化合价,进而确定还原产物解得,注意若还原产物N元素化合价为+1时,可能为N2O或NH4NO3.
解答 解:0.96g Mg的物质的量为$\frac{0.96g}{24g/mol}$=0.04mol,6.3g HNO3的物质的量为$\frac{6.3g}{63g/mol}$=0.1mol,反应生成Mg(NO3)2为0.04mol,假设0.1mol-0.04mol×2=0.02mol的HNO3全部其氧化剂作用,假设N元素咋爱还原产物中化合价为a,根据电子转移守恒,0.02mol×(5-a)=0.04mol×2,解得a=+1,故还原产物可能为N2O或NH4NO3,则还原产物的摩尔质量可能是44 g•mol-1或80 g•mol-1,
故选:B.
点评 本题考查氧化还原反应计算,注意电子转移守恒与平均值法的应用,侧重考查学生分析计算能力,难度中等.


科目:高中化学 来源: 题型:解答题
 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品、用图中的实验装置进行实验,证明过氧化钠可作供氧剂.
在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品、用图中的实验装置进行实验,证明过氧化钠可作供氧剂.| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | 除去CO2气体中混入的HCl |
| C | 石棉绒与过氧化钠 | 与CO2和水气反应,产生O2 |
| D | NaOH | 吸收未反应的CO2气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
. 该化合物属于离子(填“共价”或“离子”)化合物.
该化合物属于离子(填“共价”或“离子”)化合物.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用蒸发的方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液小火加热蒸干 | |
| B. | 配制100ml1.00mol/L的NaCl溶液,需用托盘天平准确称量5.9g氯化钠固体 | |
| C. | 利用蒸馏的方法进行乙醇与水的分离时,温度计水银球应放在液面以下来准确测定温度 | |
| D. | 用浓硫酸配制一定物质的量的浓度的稀硫酸时,向浓硫酸中加水稀释,冷却至室温后才能够移到容量瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A的质量分数增大 | B. | 化学计量数:m+n>3 | ||
| C. | 平衡向右移动 | D. | 物质C的体积分数减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 向一定物质的量浓度的AlCl3和盐酸的混合溶液中逐滴滴入NaOH溶液,生成Al(OH)3的物质的量随NaOH加入量的变化关系如图所示.则下列物质在对应的溶液中一定能大量存在的是( )
向一定物质的量浓度的AlCl3和盐酸的混合溶液中逐滴滴入NaOH溶液,生成Al(OH)3的物质的量随NaOH加入量的变化关系如图所示.则下列物质在对应的溶液中一定能大量存在的是( )| A. | a点对应的溶液中:Na+、Fe3+、SO42-、HCO3- | |
| B. | c点对应的溶液中:Na+、AlO2-、SO42-、NO3- | |
| C. | d点对应的溶液中:Ag+、Ca2+、NO3-、Cl- | |
| D. | f点对应的溶液中:K+、OH-、I-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
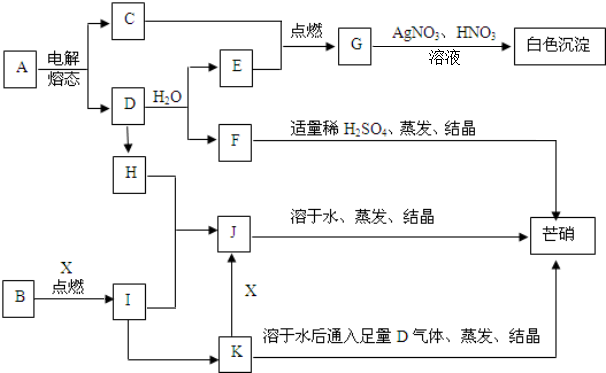
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com