
某温度下,在一容积可变的容器中,反应2A(g)+B(g)⇌2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol.保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡左移的是( )
|
| A. | 均减半 | B. | 均加倍 | C. | 均增加1mol | D. | 均减少1mol |
| 化学平衡的影响因素.. | |
| 专题: | 化学平衡专题. |
| 分析: | 在容积可变的情况下,从对平衡混合物中三者的物质的量对各物质的量的浓度影响角度思考.在“均减半”或“均加培”时,相当于A、B、C三物质的浓度都没有改变, 原平衡时A、B和C的物质的量之比为2:1:2,“均增加1mol”时相当于相当于在原来的基础上多加了B,“均减小1mol”时相当于相当于减少的A、C少,B多,以此解答该题. |
| 解答: | 解:A.由于是在容积可变的容器中,则在“均减半”相当于A、B、C三物质的浓度都没有改变,平衡不会移动,故A错误; B.由于是在容积可变的容器中,则在“均加培”相当于A、B、C三物质的浓度都没有改变,平衡不会移动,故B错误; C.如A、B和C的物质的量之比按照2:1:2的比值增加,则平衡不移动,而“均增加1mol”时相当于在原来的基础上多加了B,则平衡向右移动,故C错误; D.如A、B和C的物质的量之比按照2:1:2的比值减小,则平衡不移动,而均减少1 mol,相当于减少的A、C少,B多,则平衡左移,故D正确. 故选:D. |
| 点评: | 本题考查化学平衡移动,要注意的是基本概念、基础理论是高考中不变的一个重点.这道题的设问别具一格,解答时既要定性判断、又要定量分析,多次灵活转换,都值得大家研究,思维转化是解答该题的关键. |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列有关二元弱酸H2A的盐溶液的说法,正确的是 ( )
A.在NaHA溶液中:c(Na+)>c(HA-)>c(OH-)>c(H+)
B.在NaHA溶液中:c(Na+)>c(HA-)>c(H+)>c(OH-)
C.在Na2A溶液中c(Na+)=c(HA-)+c(OH-)+c(A2-)
D.在Na2A溶液中c(OH-)=c(H+)+c(HA-)+2c(H2A)
查看答案和解析>>
科目:高中化学 来源: 题型:
关于氧化还原反应,下列说法正确的是:
①氧化剂发生氧化反应;②氧化剂具有氧化性;③氧化反应的本质是化合价升降;④物质所含元素化合价变化是判断氧化还原反应的依据;⑤氧化还原反应的任一反应物不是氧化剂就是还原剂
A.②④ B.②③④ C.①②④ D.①②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是:
A.把100mL3mol·L-1的H2SO4跟100mLH2O混合,硫酸的物质的量浓度变为1.5mol·L-1
B.把100g20%的NaCl溶液跟100gH2O混合后,NaCl溶液的溶质质量分数是10%
C.把200mL3mol·L-1的BaCl2溶液跟100mL3mol·L-1的KCl溶液混合后, 溶液中的C(Cl-)仍然是3mol·L-1
溶液中的C(Cl-)仍然是3mol·L-1
D.把100mL20%的NaOH溶液跟100mLH2O混合后,NaO H溶液的质量分数是10%
H溶液的质量分数是10%
查看答案和解析>>
科目:高中化学 来源: 题型:
主族元素单质及化合物在许多性质上都存在着递变规律.下列有关说法不正确的是( )
|
| A. | 卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深 |
|
| B. | 氧族元素氢化物稳定性按H2O、H2S、H2Se、H2Te的顺序依次减小 |
|
| C. | 氢化物的沸点按NH3、BiH3、SbH3、AsH3、PH3的顺序依次递减 |
|
| D. | 最高价氧化物对应水化物碱性按NaOH、KOH、RbOH、CsOH的顺序依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
工业废气中氮氧化合物是造成污染的主要来源.为治污,工业上通常通入NH3与之发生下列反应:NOX+NH3→N2+H2O.现有NO、NO2的混合气3L,可用同温同压下的3.5LNH3恰好使其完全转化为N2,则原混合气体中NO和NO2的物质的量之比( )
|
| A. | 1:3 | B. | 2:1 | C. | 1:1 | D. | 1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有两只密闭容器A和B,A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时向这两个容器中分别充入等物质的量SO3气体,并使A和B容积相等(如图所示)在保持400℃的条件下使之发生如下反应:2SO2+O2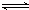 2SO3.则下列描述正确的是( )
2SO3.则下列描述正确的是( )
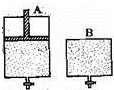
|
| A. | 达到平衡所需要的时间:A容器更短 |
|
| B. | 达到平衡时:B容器中SO3的转化率更大 |
|
| C. | 达到平衡时:A容器中SO2的物质的量更多 |
|
| D. | 达到平衡后,向两容器中分别通入等量的氦气,A容器中SO3的体积分数增大,B容器中SO3的体积分数不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是( )
|
| A. | 氯气跟水反应:Cl2+H2O=2H++Cl﹣+ClO﹣ |
|
| B. | 硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO42﹣=BaSO4↓ |
|
| C. | 碳酸钠溶液中加入少量稀盐酸:CO32﹣+H+=HCO3﹣ |
|
| D. | 铜与稀盐酸反应:Cu+2H+=Cu2++H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com