
【题目】工业中很多重要的原料都是来源于石油化工,回答下列问题

(1)C的结构简式为________。
(2)丙烯酸中含氧官能团的名称为_____________。
(3)③④反应的反应类型分别为_____________、___________。
(4)写出下列反应方程式
①反应①的化学方程式____________;
②反应②的化学方程式_________________;
③反应⑤的化学方程式____________。
(5)丙烯酸(CH2 = CH — COOH)可能发生的反应有_______________(填序号)
A 加成反应 B 取代反应 C 加聚反应 D 中和反应 E 氧化反应
(6)丙烯分子中最多有______个原子共面
【答案】CH3COOH 羧基 氧化反应 加聚反应 ![]() +HNO3
+HNO3![]() +H2O CH2=CH2+H2O
+H2O CH2=CH2+H2O![]() CH3CH2OH CH2=CH-COOH+CH3CH2OH
CH3CH2OH CH2=CH-COOH+CH3CH2OH![]() CH2=CHCOOCH2CH3+H2O ABCDE 7
CH2=CHCOOCH2CH3+H2O ABCDE 7
【解析】
分析流程图,B被高锰酸钾氧化得到C,B和C可得到乙酸乙酯,则B为乙醇,C为乙酸,所以A为乙烯,。
(1)C为乙酸,其结构简式为CH3COOH;
(2)丙烯酸中含氧官能团的名称为羧基(-COOH);
(3)反应③为氧化反应,反应④为加聚反应;
(4)反应①为苯的硝化反应,其化学方程式为![]() +HNO3
+HNO3![]() +H2O;
+H2O;
反应②为乙烯水化法制备乙醇,方程式为CH2=CH2+H2O![]() CH3CH2OH;
CH3CH2OH;
反应⑤为乙醇和丙烯酸的酯化反应,方程式为CH2=CH-COOH+CH3CH2OH![]() CH2=CHCOOCH2CH3+H2O;
CH2=CHCOOCH2CH3+H2O;
(5)丙烯酸中的官能团有碳碳双键和羧基,所以可能发生的反应有加成、取代(酯化)、加聚、中和、氧化,故答案为ABCDE;
(6)丙烯分子的结构为![]() 其中,碳碳双键上的两个碳、三个氢和甲基上的一个碳为一个平面,当甲基的角度合适时,甲基上的一个氢会在该平面内,所以最多有7个原子共平面。
其中,碳碳双键上的两个碳、三个氢和甲基上的一个碳为一个平面,当甲基的角度合适时,甲基上的一个氢会在该平面内,所以最多有7个原子共平面。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】O3能吸收有害紫外线,保护人类赖以生存的空间。O3的分子结构如图,呈V形,两个键的夹角为116.5°,三个原子以一个O原子为中心,与另外两个O原子分别构成一个共价键;中间O原子提供两个电子,旁边两个O原子各提供一个电子,构成一个特殊的化学键——三个O原子均等地享有这些电子。请回答:

(1)臭氧与氧气互为________________。
(2)下列分子与O3分子的结构最相似的是________。
A. H2O B. CO2 C. SO2 D. BeCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用加热氯酸钾的方法制取少量氧气。
(1)请写出反应的化学方程式。_____
(2)现欲制取1.12L(标准状况)氧气,理论上需要消耗氯酸钾多少克?生成氯化钾物质的量多少?______、______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为TS(中文名![]() ,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
,tián),TS的原子核外最外层电子数是7.下列说法不正确的是( )
A. TS是第七周期第ⅦA族元素 B. TS的同位素原子具有相同的电子数
C. TS在同族元素中非金属性最弱 D. 中子数为176的TS核素符号是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究含碳化合物的结构与性质,对生产、科研等具有重要意义
(1)冠醚是由多个二元醇分子之间失水形成的环状化合物。X、Y、Z是常见的三种冠醚,其结构如图所示。它们能与碱金属离子作用,并且随着环的大小不同而与不同金属离子作用。

①Li+计与X的空腔大小相近,恰好能进入到X的环内,且Li+与氧原子的一对孤电子对作用形成稳定结构W(如图)。
a.基态锂离子核外能量最高的电子所处能层符号为___________;
b.W中Li+与孤对电子之间的作用属于___________(选填字母标号)
A.离子键 B.共价键 C.配位键 D.氢键 E.以上都不是
②冠醚Y能与K+形成稳定结构,但不能与Li+计形成稳定结构。理由是___________。
③烯烃难溶于水,被KMnO4水溶液氧化的效果较差。若烯烃中溶人冠醚Z,氧化效果明显提升。
i.水分子中氧的杂化轨道的空间构型是___________,H-O键键角___________(填“>”“<”或“=”)109°28′
ii.已知:冠醚Z与KMnO4可以发生右图所示的变化。加入冠醚Z后,烯烃的氧化效果明显提升的原因是___________。
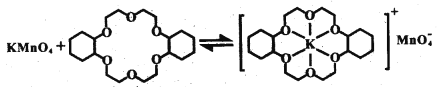
(2)甲烷是重要的清洁能源,其晶体结构如图所示,晶胞参数为anm。
①常温常压下不存在甲烷晶体。从微粒间相互作用的角度解释,其理由是___________;
②甲烷分子的配位数为___________;
③A分子中碳原子的坐标参数为(0,0,0),则B分子的碳原子的坐标参数为___________。
④甲烷晶体的密度为___________(g·cm-3)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家刚刚发现了某种元素的原子,其质量是a g,12C原子的质量是b g,NA是阿伏加德罗常数的值,下列说法正确的是( )
①该原子的摩尔质量是aNA②Wg该原子的物质的量一定是![]() mol③Wg该原子中含有
mol③Wg该原子中含有![]() 个该原子④由已知信息可得:NA=
个该原子④由已知信息可得:NA=![]()
A.①②B.③④C.②③D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个V升的密闭容器中放入2mol A(g)和1mol B(g),在一定条件下进行如下反应:3A(g)+B(g) ![]() nC(g) +2D(g),达平衡后A的浓度减小1/2,混合气体平均相对分子质量增大1/8,则该反应方程式中n的值是
nC(g) +2D(g),达平衡后A的浓度减小1/2,混合气体平均相对分子质量增大1/8,则该反应方程式中n的值是
A. 1 B. 2 C. 3 D. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知某盐酸溶液的密度为1.19g/cm3 ,质量分数为36.5%,则该溶液的物质的量浓度为___________
(2)含0.3 mol SO42-的Al2(SO4)3中所含的Al3+的数目为________________。
(3)相同质量的SO2、SO3硫原子的个数之比为_______________ 。
(4)33.3g某二价金属氯化物(ACl2)中含有0.6mol Cl,则ACl2的化学式是_________ 。
(5)标准状况下,1.204×1023个H2的体积约为_______________L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED灯是一种环保的光源,在相同照明效果下比传统光源节能80%以上。目前市售LED晶片材质基本以砷化镓、磷化铝镓钢(AlGaInP)、氮化铟镓( InGaN)为主,砷化镓的晶胞结构如图。回答下列问题:

(1)砷的基态原子的电子排布式是___________。
(2)磷和砷是同一族的元素,第一电离能:磷___________(填“>”“<”或“=”,下同)砷,它们形成的氢化物的沸点:PH3___________AsH3,原因是______________________。
(3)AsH3是无色、稍有大蒜味的气体。AsH3中砷原子的杂化轨道方式为___________,AsH3的空间结构为___________。
(4)砷元素的常见化合价有+3和+5,它们对应的含氧酸有H3AsO3和H3AsO4两种,其中H3AsO4的酸性比H3AsO3的酸性强,从物质结构与性质的关系来看,H3AsO4的酸性比H3AsO3的酸性强的原因是_________________________________。
(5)此晶胞中所含的砷原子的个数为___________,砷化镓的化学式为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com