
【题目】含磷化合物在生产生活中有着重要的应用。
(1)磷与氨是同主族元素,下列能说明者非金属性强弱的是_______(填字母)。
a.NH3比PH3稳定性强
b.常温下,氮气为气体,磷单质为固体
c.氮气与氢气化合比磷与氢气化合更困难
d.HNO3的酸性比HPO3酸性强
(2)工业常用磷精矿[Ca5(PO4)3F]和硫酸反应制各磷酸。己知25℃,101kPa时:
CaO(s)+H2SO4(l)=CaSO4(s)+H2O(l) △H=-271kJ/mol
5CaO(s)+3H3PO4(l)+HF(g)=Ca5(PO4)F(s)+5H2O(l) △H=-937kJ/mol
则Ca5(PO4)F和硫酸反应制备磷酸的热化学方程式为________________。
(3)已知PCl5(g)![]() PCl3(g)+Cl2(g)△H>0。温度为T时,把一定量的PCl5气体引入一真空瓶内,反应达平衡后PCl5与PCl3的分压之比为1:3(分压一总压×物质的量分数)。
PCl3(g)+Cl2(g)△H>0。温度为T时,把一定量的PCl5气体引入一真空瓶内,反应达平衡后PCl5与PCl3的分压之比为1:3(分压一总压×物质的量分数)。
①PCl5的分解率a1=_____%。若达到兴衡后体系总压为1.4MPa,用平衡分压代替平衡浓度表示反应的平衡常数Kp=_________。
②温度为T2时,新的平衡体系中PCl5与Cl2分压相同,则PCl5的分解率a1________a2,温度T1___T2(填“>”“<”或“=”)。
③达到平衡后,下列情况使PCl5分解率增大的是___________(填字母)。
a.温度、体积不变,充入氩气 b.体积不变,对体系加热
C.温度、体积不变,充入氯气 d.温度不变,增大容器体积
(4)氧化水解法产三氯氧磷的废水中主要含有H3PO4、H3PO3等,可先加入适量漂白粉,再加入生石灰调节pH将磷元素转化为磷酸的钙盐沉淀并回收。
①在沉淀前先加入适量漂白粉的作用是__________________。
②下图是不同条件对磷的沉淀回收率的影响图像。处理该厂废水需控制的工艺条件为______。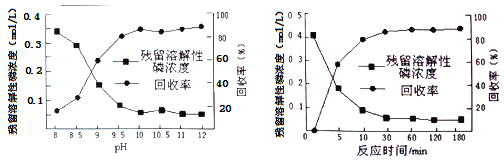
【答案】 a Ca5(PO4)3F(s) +5H2SO4(l)=5CaSO4(s)+3H3PO4(l)+HF(g) △H=﹣418kJ· mol-1 75 1.8MPa > > bd 将废水中的H3PO3氧化成H3PO4 溶液pH>10,反应时间>30min
【解析】(1)同主族元素从上到下原子序数逐渐增大,元素金属性逐渐增大,非金属性逐渐减小,单质与氢气的化合越来越难,气态氢化物稳定性逐渐减小,最高价氧化物对应的水化物的酸性逐渐减弱,所以NH3比PH3稳定性强可以说明非金属性N>P,a可以;常温下,氮气为气体,磷单质为固体是它们的物理性质,不能说明非金属性N>P,b不可以;氮气与氢气化合比磷与氢气化合更困难可以说明非金属性P>N,与元素周期律矛盾,c不可以;HPO3不是磷元素的最高价氧化物对应的水化物,所以HNO3与HPO3酸性强弱不能说明N与P非金属性强弱,d不可以;正确答案是a;
(2)根据盖斯定律:将CaO(s)+H2SO4(l)=CaSO4(s)+H2O(l) △H=-271kJ/mol乘以5倍减去
5CaO(s)+3H3PO4(l)+HF(g)=Ca5(PO4)F(s)+5H2O(l) △H=-937kJ/mol得到:Ca5(PO4)3F(s) +5H2SO4(l)=5CaSO4(s)+3H3PO4(l)+HF(g) △H=﹣418kJ· mol-1,所以Ca5(PO4)F和硫酸反应制备磷酸的热化学方程式为:Ca5(PO4)3F(s) +5H2SO4(l)=5CaSO4(s)+3H3PO4(l)+HF(g) △H=﹣418kJ· mol-1;
(3) 假设一定量的PCl5为amol,压强是P0
PCl5(g)![]() PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
开始(mol) a 0 0
转化(mol) x x x
平衡(mol) a-x x x
根据:分压=总压×物质的量分数,达平衡后P(总)=(a+x)P0/a,P(PCl5)=(a-x)P(总)/(a+x), P(Cl2)= P(PCl3)=xP(总)/(a+x),根据反应达平衡后PCl5与PCl3的分压之比为1:3得出:x=3a/4;
① PCl5的分解率a1=x/a=75% , 平衡分压代替平衡浓度表示反应的平衡常数表达式是:Kp=P(Cl2)P(PCl3)/P(PCl5),将P(总)=1.4MPa代入得:Kp=1.8MPa
② 根据①的计算数据可知,在原平衡中,P(PCl5)<P(Cl2),新平衡中两者相同,说明平衡逆向移动,根据反应方程式:PCl5(g)![]() PCl3(g)+Cl2(g)△H>0,该反应正反应是吸热反应,平衡逆向移动,说明温度降低,即T2<T1,新平衡与原平衡相比,PCl5分解率降低了,所以正确答案是:a1>a2,温度T1>T2;
PCl3(g)+Cl2(g)△H>0,该反应正反应是吸热反应,平衡逆向移动,说明温度降低,即T2<T1,新平衡与原平衡相比,PCl5分解率降低了,所以正确答案是:a1>a2,温度T1>T2;
③ PCl5(g)![]() PCl3(g)+Cl2(g)△H>0达到平衡后,温度、体积不变,充入氩气,反应物、生成物的浓度都没有改变,平衡不移动,a不能使PCl5分解率增大,a选项错误;体积不变,对体系加热,相当于升高温度,该反应的正反应是吸热反应,平衡正向移动,能使PCl5分解率增大,所以b选项正确;温度、体积不变,充入氯气,平衡逆向移动,PCl5分解率减小,c选项错误;温度不变,增大容器体积,平衡正向移动,能使PCl5分解率增大,d选项正确;所以达到平衡后,使PCl5分解率增大的选项是bd;
PCl3(g)+Cl2(g)△H>0达到平衡后,温度、体积不变,充入氩气,反应物、生成物的浓度都没有改变,平衡不移动,a不能使PCl5分解率增大,a选项错误;体积不变,对体系加热,相当于升高温度,该反应的正反应是吸热反应,平衡正向移动,能使PCl5分解率增大,所以b选项正确;温度、体积不变,充入氯气,平衡逆向移动,PCl5分解率减小,c选项错误;温度不变,增大容器体积,平衡正向移动,能使PCl5分解率增大,d选项正确;所以达到平衡后,使PCl5分解率增大的选项是bd;
(4)①氯化水解法生产三氯氧磷会产生含磷(主要为H3PO4、H3PO3等)废水,在废水中先加入适量漂白粉,使废水中的H3PO3氧化为PO43-,加入生石灰后能完全转化为磷酸的钙盐,达到较高的回收率;
②根据题干中的图可确定pH≥10,磷的沉淀回收率较高(90%左右),反应时间超过30 min时磷的沉淀回收率较高((90%左右),所以处理该厂废水最合适的工艺条件为溶液pH>10,反应时间>30min。


科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol
B.CO(g)的燃烧热是283.0 kJ/mol,则2CO(g)+O2(g) =2CO2(g)反应的ΔH=—(2×283.0)kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用电化学法制备LiOH的实验装置如图,采用惰性电极,a口导入LiCl溶液,b口导入LiOH溶液,下列叙述正确的是( )

A.通电后阳极区溶液pH增大
B.阴极区的电极反应式为4OH-–4e-=O2↑+2H2O
C.当电路中通过1mol电子的电量时,会有0.25mol的Cl2生成
D.通电后Li+通过交换膜向阴极区迁移,LiOH浓溶液从d口导出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解法合成氨因其原料转化率大幅度提高,有望代替传统的工业合成氨工艺。电解法合成氨的两种原理及装置如图1和图2所示。
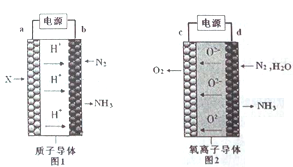
下列说法错误的是
A. a电极上通入的物质是H2
B. 电解池中b是阳极,c是阴极
C. d电极上电极反应式是N2+3H2O+6e-=2NH3+3O2-
D. 若I=2.0A,通电1h,理论上两装置均可得NH3的质量为![]() 。(已知一个电子的电量为1.6×10-19C)
。(已知一个电子的电量为1.6×10-19C)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下向100mL0.2mol/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液中NH4+和NH3·H2O的物质的量分数φ与加入盐酸的体积V及混合液pH变化的关系如图所示,下列说法正确的是

A. 表示NH3·H2O物质的量分数变化的曲线是B
B. pH=9.26时的溶液中,NH3·H2O的电离程度小于NH4+的水解程度
C. 常温下,NH3·H2O的电离常数为1.8×10-5mol/L(已知lg1.8=0.26)
D. 当加入盐酸体积为50mL时,溶液中c(NH4+)-c(NH3·H2O)=2×(10-5+10-9)mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是由苯乙烯为原料合成有机高分子化合物M的一种合成路线(部分反应条件及副产物已略去):

已知:I.RCHBr-CH2Br![]() RC≡CH
RC≡CH
II.CH≡CH+CH2=CH-CH=CH2![]()
III. 
请回答下列问题:
(1)D的结构简式为______,E的结构简式为________。
(2)C+D→E的反应类型为______,I中含氧官能团的名称为___________。
(3)H+I→M的化学方程式为___________。
(4)在催化剂加热条件下,G与氧气反应生成Q(C9H8O3),同时满足下列条件的Q的同分异构体有_____种(不考虑立体异构),其中核磁共振氢谱有6组吸收峰的结构简式为____。
①除苯环外不含其他环状结构
②能与FeCl3溶液发生显色反应
③能与NaHCO3溶液反应生成CO2
(5)参照上述合成路线和相关信息,以甲醇和一氯环己烷为有机原料(无机试剂任选),设计制备己二酸二甲酯的合成路线_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学化学常见的滴定法包括中和滴定法、氧化还原反应滴定法等。
(1)探究小组甲用酸性KMnO4溶液滴定某补血剂[主要成分硫酸亚铁晶体(FeSO47H2O)]中铁元素的含量。
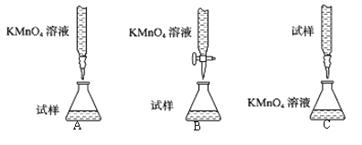
①下列滴定装置中(夹持部分略去),最合理的是:__________(填字母序号)。
②该小组拟在同浓度的FeSO4溶液中,探究酸性KMnO4溶液浓度对Fe2+被氧化时反应速率的影响。限选试剂与仪器:0.10molL-1FeSO4、0.02molL-1酸性KMnO4、蒸馏水、锥形瓶、试管、胶头滴管、量筒、秒表。参照下表格式,完成实验表格(列出所选试剂体积和数据;数据用字母表示)。_____________、_____________、_____________、_____________。

(2)常温下,探究小组乙将0.1 mol·L-1盐酸滴入20 mL 0.1 mol·L-1氨水中,溶液的pH随加入盐酸体积的变化曲线如图所示。
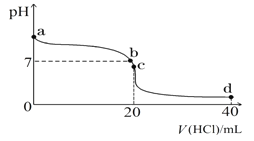
①a点处假设溶液的pH=10,则该点处由水电离产生的c(OH-)=__________________。
②取c点时的饱和溶液并向其加入水玻璃(硅酸钠水溶液),振荡、静置。写出实验现象并用必要的文字和相关离子方程式给予解释:___________________________________。
③d点所示溶液中离子浓度由大到小的排序是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. 一定条件下反应2SO2+O2![]() 2SO3达到平衡时,v(O2)正=2v(SO3)逆
2SO3达到平衡时,v(O2)正=2v(SO3)逆
B. 用如图所示方法可保护钢闸门不被腐蚀

C. 常温下,向NH4Cl溶液中加入少量NaOH固体,溶液中![]() 的值增大
的值增大
D. 常温下, pH=2的HCl溶液与pH=12的Ba(OH)2溶液等体积混合,两者恰好完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是一种治疗帕金森症的药品,其合成路线流程图如下:
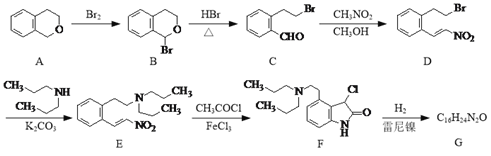
(1)D中的官能团名称为溴原子、______和______。
(2)B、C、D三种有机物与NaOH乙醇溶液共热,能发生消去反应的是____(填字母)。
(3)写出同时满足下列条件的D的一种同分异构体的结构简式:______。
①分子中只有3种不同化学环境的氢;
②能发生银镜反应,苯环上的一取代物只有一种。
(4)F通过取代反应得到G,G的分子式为C16H24N2O,写出G的结构简式:______。
(5)已知:![]() (R代表烃基或H)。
(R代表烃基或H)。
请写出以![]() 和CH3NO2为原料制备
和CH3NO2为原料制备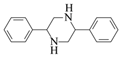 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。__________________
的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。__________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com