
”¾ĢāÄæ”æ±ź×¼×“æöĻĀV LµÄHClĘųĢåČܽāŌŚ1LĖ®ÖŠ£ØĖ®µÄĆÜ¶Č½üĖĘĪŖ1g/mL£©£¬ĖłµĆČÜŅŗµÄĆܶČĪŖ¦Ń g/mL£¬ÖŹĮæ·ÖŹżĪŖ¦Ų£¬ĪļÖŹµÄĮæÅضČĪŖc mol/L£¬ŌņĻĀĮŠ¹ŲĻµÖŠ²»ÕżČ·µÄŹĒ£Ø £©
A.c= ![]()
B.¦Ų= ![]()
C.¦Ų= ![]()
D.¦Ń= ![]()
”¾“š°ø”æD
”¾½āĪö”æ½ā£ŗA£®HClĪļÖŹµÄĮæĪŖ ![]() mol£¬ĘäÖŹĮæĪŖ
mol£¬ĘäÖŹĮæĪŖ ![]() mol”Į36.5g/mol=
mol”Į36.5g/mol= ![]() g£¬1LĖ®µÄÖŹĮæĪŖ1000g£¬¼ĘĖćČÜŅŗÖŹĮæĪŖ£ŗ£Ø1000+
g£¬1LĖ®µÄÖŹĮæĪŖ1000g£¬¼ĘĖćČÜŅŗÖŹĮæĪŖ£ŗ£Ø1000+ ![]() £©g£¬ŌņČÜŅŗĢå»żĪŖ
£©g£¬ŌņČÜŅŗĢå»żĪŖ ![]() =
= ![]() L£¬¹ŹČÜŅŗÅضČc=
L£¬¹ŹČÜŅŗÅضČc= 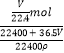 =
= ![]() mol/L£¬¹ŹAÕżČ·£»
mol/L£¬¹ŹAÕżČ·£»
B£®ČÜÖŹÖŹĮæ·ÖŹż=  =
= ![]() £¬¹ŹBÕżČ·£»
£¬¹ŹBÕżČ·£»
C£®øł¾Żc= ![]() æÉÖŖ¦Ų=
æÉÖŖ¦Ų= ![]() £¬¹ŹCÕżČ·£»
£¬¹ŹCÕżČ·£»
D£®¦Ń= ![]() =
= ![]() £¬ČÜŅŗĢå»żĪŖ£ØV+1£©L£¬¶ųČÜŅŗĢå»ż²»µČÓŚĘųĢåĢå»żÓėĖ®µÄĢå»żÖ®ŗĶ£¬¹ŹD“ķĪó£¬
£¬ČÜŅŗĢå»żĪŖ£ØV+1£©L£¬¶ųČÜŅŗĢå»ż²»µČÓŚĘųĢåĢå»żÓėĖ®µÄĢå»żÖ®ŗĶ£¬¹ŹD“ķĪó£¬
¹ŹŃ”D£®


 ĆūŠ£Į·æ¼¾ķĘŚÄ©³å“Ģ¾ķĻµĮŠ“š°ø
ĆūŠ£Į·æ¼¾ķĘŚÄ©³å“Ģ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ŹĒŌŖĖŲÖÜĘŚ±ķµÄŅ»²æ·Ö£¬¹ŲÓŚŌŖĖŲX£¬Y£¬ZµÄŠšŹöÕżČ·µÄŹĒ£Ø £©
¢ŁXµÄĘųĢ¬Ēā»ÆĪļÓėYµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļÄÜ·¢Éś·“Ӧɜ³ÉŃĪ£»
¢ŚY£¬ZµÄĘųĢ¬Ēā»ÆĪļĖ®ČÜŅŗµÄĖįŠŌY£¼Z£»
¢ŪZµÄµ„ÖŹ³£ĪĀĻĀŹĒŅŗĢ壬æÉÓėĢś·Ū·“Ó¦£»
¢ÜZµÄŌ×ÓŠņŹż±ČY“ó19£»
¢ŻZĖłŌŚµÄÖÜĘŚÖŠŗ¬ÓŠ32ÖÖŌŖĖŲ£®
A.¢Ł¢Ś¢Ū¢Ü
B.¢Ł¢Ś¢Ū¢Ü¢Ż
C.Ö»ÓŠ¢Ū
D.Ö»ÓŠ¢Ł¢Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»¶ØĪĀ¶ČĻĀ£¬½«ĘųĢåXŗĶĘųĢåYø÷0.16mol³äČė10LŗćČŻĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦
X(g) + Y(g)![]() 2Z(g) ”÷H < 0£¬Ņ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā”£·“Ó¦¹ż³ĢÖŠ²ā¶ØµÄŹż¾ŻČēĻĀ±ķ£ŗ
2Z(g) ”÷H < 0£¬Ņ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā”£·“Ó¦¹ż³ĢÖŠ²ā¶ØµÄŹż¾ŻČēĻĀ±ķ£ŗ
t /min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®·“Ó¦Ē°2minµÄĘ½¾łĖŁĀŹv(Z) =4.0”Į10-3mol/(Lmin)
B£®ĘäĖūĢõ¼ž²»±ä£¬½µµĶĪĀ¶Č£¬·“Ó¦“ļµ½ŠĀĘ½ŗāĒ°v(Äę) > v(Õż)
C£®øĆĪĀ¶ČĻĀ“Ė·“Ó¦µÄĘ½ŗā³£ŹżK=1.44
D£®ĘäĖūĢõ¼ž²»±ä£¬ŌŁ³äČė0.2molZ£¬Ę½ŗāŹ±XµÄĢå»ż·ÖŹżŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫6.50gŠæĶ¶Čė200mLijÅØ¶ČµÄŃĪĖįÖŠ£¬ŠæŗĶŃĪĖįĒ”ŗĆĶźČ«·“Ó¦£®Ēó£ŗ
£Ø1£©6.50gŠæµÄĪļÖŹµÄĮæĪŖ¶ąÉŁ£æ
£Ø2£©·“Ó¦ÖŠÉś³ÉµÄH2ŌŚ±ź×¼×“æöĻĀµÄĢå»żĪŖ¶ąÉŁ£æ
£Ø3£©ĖłÓĆŃĪĖįÖŠHClµÄĪļÖŹµÄĮæÅضČĪŖ¶ąÉŁ£æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ25”ę”¢101 kPaĻĀ£¬ČēĻĀĶ¼ĖłŹ¾£¬ŹÆÄ«µÄČ¼ÉÕČČĪŖŅ»393.51 kJ”¤mol-1£¬½šøÕŹÆµÄČ¼ÉÕČČĪŖŅ»395.4kJ”¤mol-1”£ĻĀĮŠ±ķ“ļÕżČ·µÄŹĒ

A. ½šøÕŹÆ±ČŹÆÄ«ĪȶØ
B. C(s”¢ŹÆÄ«)£½C(s”¢½šøÕŹÆ) ”÷H£½£«1.9 kJ/mol
C. ”÷H1£¼”÷H2
D. Čē¹ūŹ¹ÓĆ“ß»Æ¼Į£¬”÷H1ŗĶ”÷H2¶¼±äŠ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫¶žŃõ»ÆĮņĘųĢåĶØČėKIO3µķ·ŪČÜŅŗ£¬ČÜŅŗĻȱ䥶ŗóĶŹÉ«”£“Ė¹ż³ĢÖŠ¶žŃõ»ÆĮņ±ķĻÖ³ö
A. ĖįŠŌB. Ęư׊ŌC. Ńõ»ÆŠŌD. »¹ŌŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ŌÓŚ¢ōA×åŌŖĖŲ£¬ĻĀĮŠŠšŹöÖŠ²»ÕżČ·µÄŹĒ(””””)
A. CO2ŌŚ³£ĪĀĻĀŹĒĘųĢ壬SiO2ŌŚ³£ĪĀĻĀŹĒ¹ĢĢå
B. C”¢Si”¢GeµÄ×īĶā²ćµē×ÓŹż¶¼ŹĒ4£¬“ĪĶā²ćµē×ÓŹż¶¼ŹĒ8
C. CO2ŗĶSiO2¶¼ŹĒĖįŠŌŃõ»ÆĪļ£¬ŌŚŅ»¶ØĢõ¼žĻĀ¶¼ÄÜŗĶŃõ»ÆøĘ·“Ó¦
D. øĆ×åŌŖĖŲµÄÖ÷ŅŖ»ÆŗĻ¼ŪŹĒ£«4ŗĶ£«2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ0.1mol/L°±Ė®ČÜŅŗµÄpH =a£¬ĻĀĮŠÄÜŹ¹ČÜŅŗpH =£Øa -1£©µÄ“ėŹ©ŹĒ
A. ½«ČÜŅŗĻ”ŹĶµ½ŌĢå»żµÄ10±¶B. ¼ÓČėŹŹĮæµÄĀČ»Æļ§¹ĢĢå
C. ¼ÓČėµČĢå»ż0.1 mol/LÉÕ¼īČÜŅŗD. ¼ÓČėµČĢå»ż0.1 mol/LŃĪĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¼õÉŁµŖµÄŃõ»ÆĪļŗĶĢ¼µÄŃõ»ÆĪļŌŚ“óĘųÖŠµÄÅÅ·ÅŹĒ»·¾³±£»¤µÄÖŲŅŖÄŚČŻÖ®Ņ»”£
£Ø1£©ŅŃÖŖ£ŗN2(g)£«O2(g)£½2NO(g) ¦¤H£½£«180.5kJ”¤mol-1
C(s)£«O2(g)£½CO2(g) ¦¤H£½£393.5 kJ”¤mol-1
2C(s)£«O2(g)£½2CO(g) ¦¤H£½£221 kJ”¤mol-1
Čōij·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖ£ŗK£½ £¬ĒėŠ“³ö“Ė·“Ó¦µÄČČ»Æѧ·½³ĢŹ½________”£
£¬ĒėŠ“³ö“Ė·“Ó¦µÄČČ»Æѧ·½³ĢŹ½________”£
£Ø2£©ÓĆCH4“߻ƻ¹ŌNOxæÉŅŌĻū³żĪŪČ¾£¬Čō½«·“Ó¦CH4£«2NO2£½CO2£«2H2O£«N2Éč¼ĘĪŖŌµē³Ų£¬µē³ŲÄŚ²æŹĒ²ōŌÓŃõ»ÆīʵÄŃõ»Æļƾ§Ģ壬æÉŅŌ“«µ¼O2-£¬ŌņøƵē³ŲµÄÕż¼«·“Ó¦Ź½ĪŖ________”£
£Ø3£©ĄūÓĆH2ŗĶCO2ŌŚŅ»¶ØĢõ¼žĻĀæÉŅŌŗĻ³ÉŅŅĻ©£ŗ6H2(g)£«2CO2(g) ![]() CH2=CH2(g)£«4H2O(g)”£ŅŃÖŖ²»Ķ¬ĪĀ¶Č¶ŌCO2µÄ×Ŗ»ÆĀŹ¼°“߻ƼĮµÄŠ§ĀŹÓ°ĻģČēÓŅĶ¼ĖłŹ¾£¬ĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ________£ØĢīŠņŗÅ£©”£
CH2=CH2(g)£«4H2O(g)”£ŅŃÖŖ²»Ķ¬ĪĀ¶Č¶ŌCO2µÄ×Ŗ»ÆĀŹ¼°“߻ƼĮµÄŠ§ĀŹÓ°ĻģČēÓŅĶ¼ĖłŹ¾£¬ĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ________£ØĢīŠņŗÅ£©”£

¢Ł²»Ķ¬Ģõ¼žĻĀ·“Ó¦£¬NµćµÄĖŁĀŹ×ī“ó
¢ŚMµćŹ±Ę½ŗā³£Źż±ČNµćŹ±Ę½ŗā³£Źż“ó
¢ŪĪĀ¶ČµĶÓŚ250”ꏱ£¬ĖęĪĀ¶ČÉżøßŅŅĻ©µÄ²śĀŹŌö“ó
¢ÜŹµ¼Ź·“Ó¦Ó¦¾”æÉÄÜŌŚ½ĻµĶµÄĪĀ¶ČĻĀ½ųŠŠ£¬ŅŌĢįøßCO2µÄ×Ŗ»ÆĀŹ
£Ø4£©ŌŚĆܱÕČŻĘ÷ÖŠ³äČė5 mol COŗĶ4 mol NO£¬·¢ÉśÉĻŹö£Ø1£©ÖŠÄ³·“Ó¦£¬ĻĀĶ¼ĪŖĘ½ŗāŹ±NOµÄĢå»ż·ÖŹżÓėĪĀ¶Č”¢Ń¹ĒæµÄ¹ŲĻµ”£

»Ų“šĻĀĮŠĪŹĢā£ŗ
¢ŁĪĀ¶Č£ŗT1________T2£ØĢī”°£¼”±»ņ”°£¾”±£©”£
¢ŚÄ³ĪĀ¶ČĻĀ£¬Čō·“Ó¦½ųŠŠµ½10·ÖÖÓ“ļµ½Ę½ŗāדĢ¬DµćŹ±£¬ČŻĘ÷µÄĢå»żĪŖ2 L£¬Ōņ“ĖŹ±µÄĘ½ŗā³£ŹżK£½________£Ø½į¹ū¾«Č·µ½Į½Ī»Š”Źż£©£»ÓĆCOµÄÅØ¶Č±ä»Æ±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁĀŹv(CO)£½________”£
¢ŪČōŌŚDµć¶Ō·“ӦȯĘ÷ÉżĪĀµÄĶ¬Ź±Ą©“óĢå»żÖĮĢåĻµŃ¹Ēæ¼õŠ”£¬ÖŲŠĀ“ļµ½µÄĘ½ŗāדĢ¬æÉÄÜŹĒĶ¼ÖŠA”«GµćÖŠµÄ________µć”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com