
【题目】已知元素X、Y原子序数均不大于20。某含氧酸盐甲的化学式为XYO3。请回答:
(1)若常温下Y的单质能与水发生反应,X原子序数大于Y,则X位于周期表的_____,X、Y形成简单离子半径大小关系为X______(填“大于”“小于”或“等于”)Y。395℃时,甲能发生分解反应生成两种盐,一种是含Y元素的无氧酸盐,该反应的化学方程式是_____________。
(2)若甲灼烧时,火焰呈现砖红色,且与盐酸反应时产生有刺激性气味气体。则甲为__(填化学式)。该气体能使高锰酸钾溶液褪色,反应的离子方程式为_____。
(3)若X、Y是不同周期的短周期元素,甲与盐酸反应逸出无色无味气体乙。
则:①乙中所含化学键类型为_______。
②该反应的离子方程式为______。
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
【题目】目前海水提溴的最主要方法之一是空气吹出法,工艺流程如下:

以下推断不合理的是
A.流程中循环利用的物质有SO2、Br2、Cl2,等多种
B.SO2吸收溴的反应方程式:SO2+2H2O+Br2=H2SO4+2HBr
C.空气能吹出溴是利用溴易挥发的性质
D.没有采用直接蒸馏含溴海水得到单质溴的主要原因是为了节能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定0.1 mol·L-1 Na2SO3溶液先升温再降温过程中的pH,数据如下。
时刻 | ① | ② | ③ | ④ |
温度/℃ | 25 | 30 | 40 | 25 |
pH | 9.66 | 9.52 | 9.37 | 9.25 |
实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比实验,④产生白色沉淀多。
下列说法不正确的是
A. Na2SO3溶液中存在水解平衡:![]() +H2O
+H2O![]()
![]() +OH
+OH
B. ④的pH与①不同,是由于![]() 浓度减小造成的
浓度减小造成的
C. ①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
D. ①与④的Kw值相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定![]() 溶液先升温再降温过程中的pH,数据如下。实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比实验。④产生白色沉淀多。下列说法不正确的是
溶液先升温再降温过程中的pH,数据如下。实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比实验。④产生白色沉淀多。下列说法不正确的是![]()
![]()
时刻 | ① | ② | ③ | ④ |
温度 | 25 | 30 | 40 | 25 |
pH |
|
|
| 9.25 |
A.![]() 溶液中存在水解平衡:
溶液中存在水解平衡:![]()
B.④的pH与①不同,是由于![]() 浓度减小造成的
浓度减小造成的
C.①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
D.①与④的![]() 值相等
值相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向20mL0.1mol/LNaOH溶液中逐滴加入0.1mol/L![]() 溶液,溶液的pH与所加
溶液,溶液的pH与所加![]() 溶液的体积关系如图所示,下列说法正确的是
溶液的体积关系如图所示,下列说法正确的是
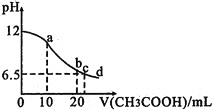
A.进行该实验时,温度高于![]()
B.a点溶液中:![]()
C.c点溶液中:![]()
D.![]() 过程中,水的电离程度始终逐渐增大
过程中,水的电离程度始终逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,水溶液中H+和OH-的浓度变化曲线如图。下列说法正确的是( )

A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,加入FeCl3可能引起由b向a的变化
D.该温度下,稀释溶液可能引起由c向d的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]() ,
,![]() 。
。![]() 时,向
时,向![]() 溶液中滴加氢氧化钠溶液,混合溶液的pOH与
溶液中滴加氢氧化钠溶液,混合溶液的pOH与![]() 的变化关系如图所示。下列叙述正确的是
的变化关系如图所示。下列叙述正确的是

A.M点溶液中:![]()
B.![]() 的数量级为
的数量级为![]()
C.M点到N点: 的值不变
的值不变
D.N点:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物结构如图,下列说法中正确的是![]()
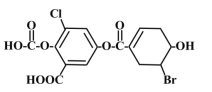
A. 该物质的化学式为C15H8O8BrCl
B. 该物质能与![]() 溶液发生显色反应
溶液发生显色反应
C. 1mol该物质最多能与3mol溴水发生加成反应
D. 一定条件下,1mol该物质最多能与8molNaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为反应2H2(g)+O2(g)=2H2O(g)的能量变化示意图。下列说法正确的是
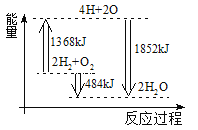
A. 拆开2molH2 (g)和1 molO2(g)中的化学键成为H、O原子,共放出1368 kJ能量
B. 由H、O原子形成2 molH2O(g),共吸收1852 kJ能量
C. 2 molH2 (g)和1 molO2 (g)反应生成2 molH2O(1),共吸收484 kJ能量
D. 2 molH2 (g)和1 molO2(g)反应生成2 moIH2O(g),共放出484 kJ能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com