
【题目】(1)写出浓硫酸与木炭粉在加热条件下反应的化学方程式 _。
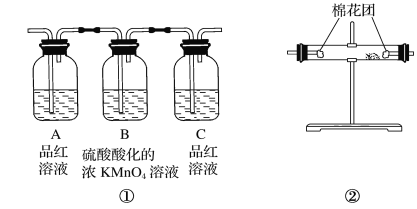
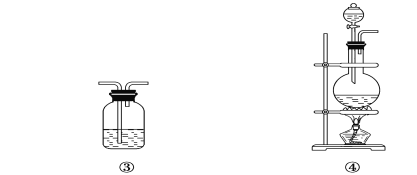
(2)试用上图所示各装置设计一个实验,验证上述反应所产生的各种产物。这些装置的连接顺序(按产物气体从左至右的流向)是________→________→________→________(填装置的编号)。
(3)怎样检查整套装置的气密性
(4)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色,A瓶溶液的作用是________,B瓶溶液的作用是________,C瓶溶液的作用是________。
(5)装置②中所加的固体药品是________,可验证的产物是________。
(6)装置③中所盛溶液是________,可验证的产物是________。
【答案】(1)C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O(2分)
CO2↑+2SO2↑+2H2O(2分)
(2)④ ② ① ③(2分)
(3)关闭分液漏斗活塞,微热烧瓶,③导管口产生气泡,停止加热后③导管中有一段稳定的液柱,则气密性良好(2分)
(4)验证SO2的存在(1分) 充分吸收SO2(1分) 验证SO2是否已被吸收完全(1分)
(5)无水硫酸铜(1分) 水(1分)(6)澄清的石灰水(1分) CO2(1分)
【解析】
试题分析:(1)碳可以和浓硫酸反应生成二氧化碳、二氧化硫以及水,反应的方程式为C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O;
CO2↑+2SO2↑+2H2O;
(2)检验二氧化碳和二氧化硫时用到的溶液中均含有水,所以先检验水的存在,二氧化碳和二氧化硫均可以使澄清石灰水变浑浊,所以先检验二氧化硫,再除去,最后检验二氧化碳,连接顺序④→②→①→③;
(3)根据装置结构可知检验气密性的实验操作是:关闭分液漏斗活塞,微热烧瓶,③导管口产生气泡,停止加热后③导管中有一段稳定的液柱,则气密性良好。
(4)根据检验的顺序,在检验二氧化碳之前先检验二氧化硫,可以用品红来检验,除二氧化硫可以用高锰酸钾,二氧化硫是否被高锰酸钾吸收干净,也可以用品红来检验,所以A瓶溶液的作用是验证SO2的存在,B瓶溶液的作用是充分吸收SO2,C瓶溶液的作用是验证SO2是否已被吸收完全;
(5)根据以上分析可知用无水硫酸铜来检验水的产生,则装置②中所加的固体药品是无水硫酸铜。
(6)根据以上分析可知可以用澄清石灰水检验二氧化碳的存在,因此装置③中所盛溶液是澄清的石灰水。


科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,表中所列字母分别代表某一元素。根据表中所列元素回答下列问题:

(1)元素d在周期表中的位置是_____________,h与f原子序数相差______________。
(2)b、c、f的简单离子半径最小的是___________(填离子符号),原子半径最小的是______(填化学式)。
(3)表中第三周期元素的非金属性最强是_________(用元素符号表示), e、f、g三种元素的气态氢化物最不稳定的是__________(用化学式表示)。
(4)g元素与b元素的最高价氧化物对应水化物反应的化学方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为检验浓硫酸与木炭在加热条件下反应产生SO2和CO2气体,设计了如图11所示实验装置,a、b、c为止水夹,B是用于储气的气囊,D中放有用I2和淀粉的蓝色溶液浸湿的脱脂棉。

请回答下列问题:
(1)实验前欲检查装置A的气密性,可以采取的操作是_______________。
(2)此实验成败的关键在于控制反应产生气体的速率不能过快,由此设计了虚框部分的装置,则正确的操作顺序是______________(用操作编号填写);
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热;
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b;
③打开止水夹a和c,关闭止水夹b;
(3)实验时,装置C中的现象为___________________________;
(4)当D中产生____________现象时,可以说明使E中澄清石灰水变浑的是CO2,而不是SO2;
A.进气口一端脱脂棉蓝色变浅,出气口一端脱脂棉蓝色不变
B.脱脂棉上蓝色均变浅
C.脱脂棉上蓝色褪去
D.脱脂棉上蓝色不变
则装置D的作用为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某次采集酸雨样品,每隔一段时间测定一次pH,得到数据如下:
时间 | 开始 | 8小时 | 16小时 | 24小时 | 32小时 | 40小时 | 48小时 |
pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
(1)放置时,雨水样品酸性_______________(填“增强”、“减弱”或“不变”)。
酸性变化的原因_________________________________(用化学方程式表示)。
II.汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源。冶理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(2) 写出一氧化碳与一氧化氮反应的化学方程式:__________________________。
(3) 在“催化转化器”转化后的气体中有CO2、SO2,下列不能鉴别这两种气体的是(____)
A.KMnO4溶液 B.石灰水 C.BaCl2溶液 D.品红溶液
(4) 有效减少城市污染的方法可以有____________
A. 开发氢能源 B. 使用电动车 C. 植树造林 D. 戴上呼吸面具
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列防止金属腐蚀的方法属于电化学防护的是
A. 船体表面刷漆 B. 水中的钢闸门连接电源的负极
C. 自行车链条涂油 D. 加入铬、锰、硅等制成不锈钢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某反应为


(1)1 mol M完全燃烧需要________ mol O2。
(2)有机物N不能发生的反应为________(填字母序号)。
A.氧化反应
B.取代反应
C.消去反应
D.还原反应
E.加成反应
(3)M有多种同分异构体,其中能使FeCl3溶液显紫色、苯环上只有两个取代基、无环物质的同分异构体有________种。
(4)物质N与H2反应生成的P(结构简式为 )发生缩聚反应产物的结构简式为________________;P物质的钠盐在适当条件下氧化为芳香醛Q,则Q与银氨溶液发生反应的化学方程式为______________________________。
)发生缩聚反应产物的结构简式为________________;P物质的钠盐在适当条件下氧化为芳香醛Q,则Q与银氨溶液发生反应的化学方程式为______________________________。
(5)有机物Ⅰ、Ⅱ、Ⅲ的转化关系为Ⅰ Ⅱ
Ⅱ
有机物Ⅱ的结构简式为______________;A、B可以发生类似①的反应生成有机物Ⅰ,则该反应的化学方程式为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图所示实验装置进行相应实验,能达到实验目的的是( )

A.用图①所示装置,蒸干NH4Cl饱和溶液制备NH4Cl晶体
B.按装置②所示的气流方向可用于收集H2、NH3等
C.用图③所示装置,分离CCl4萃取I2水后的有机层和水层
D.用图④所示装置,可以证明氧化性:Cl2>Br2>I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三草酸合铁酸钾晶体K3[Fe(C2O4)3]·3H2O可用于摄影和蓝色印刷,它受热易分解,为了验证其气态产物,某同学设计了如下实验装置:
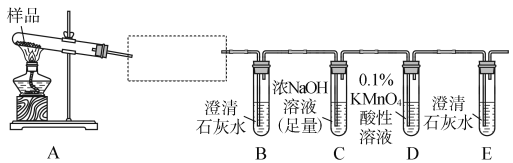
(1)若实验中,观察到B、E中的溶液均变浑浊,则D中的现象是_______________________;
说明其气态产物是________、________;为验证另一种气态产物,应在A、B之间增加的装置为________。
(2)为了使实验更安全、更严密,你认为该实验设计需要如何改进?
①______________________________;
②__________________________________。
(3)固体产物中铁元素不可能以+3价形式存在,理由是___________________________。
现设计实验,探究固体产物中铁元素的存在形式。
①提出合理假设。
假设1:_________________________________;
假设2:_________________________________;
假设3:_________________________________。
②某学生设计实验探究上述假设,除3%H2O2、蒸馏水外,还需要下列试剂中的____________________________。
限选试剂:浓硫酸、1.0 mol·L-1HNO3、1.0 mol·L-1盐酸、1.0 mol·L-1NaOH溶液、0.1 mol·L-1KI溶液、0.1 mol·L-1CuSO4溶液、20%KSCN溶液。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com