
下图为含有少量Zn杂质的粗银电解精炼银的示意图
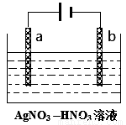
(1) (填a或b)极为含有杂质的粗银。
(2)电解一段时间后电解液中c(Ag+)浓度________(填偏大,偏小或不变)。
(3)若b极有少量红棕色气体生成,则生成该气体的电极反应式为 。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015-2016学年江苏省高一创新班下期末化学试卷(解析版) 题型:填空题
(1)某温度(t℃)时,测得0.01mol/L的NaOH溶液的pH=11,则该温度下水的KW=_______。在此温度下,将pH=a的NaOH溶液Va L与pH=b的H2SO4溶液Vb L混合,若所得混合液为中性,且a+b=12,则Va:Vb=___________。
(2)25℃时,0.1mol/L的HaA溶液中c(H+)/c(OH-)=1010,请回答下列问题:
①HaA是___________(填“强电解质”或“弱电解质”)。
②在加水稀释HaA溶液的过程中,随着水量的增加而增大的是__________(填字母)
A.c(HaA) B.c(H+)/c(HaA) C.c(H+)与c(OH-)的乘积 D.c(OH-)
③NanA溶液显__________(填“酸性”、“中性”或“碱性”),理由是(用离子方程式表示)____________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川成都外国语学校高一下期末理科化学卷(解析版) 题型:选择题
下列有关物质性质的比较正确的是
①同主族元素的单质从上到下,氧化性逐渐减弱,熔点逐渐升高
②元素的非金属性越强,气态氢化物的热稳定性越弱
③单质与水反应的剧烈程度:F2>Cl2>Br2>I2
④元素的非金属性越强,它的气态氢化物水溶液的酸性越强
⑤还原性:S2﹣>Se2﹣
⑥酸性:HNO3>H3PO4.
⑦原子半径:K>Cl>S>O>F
A. ①③ B. ②④⑦ C. ③⑥ D. ⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高一下期末化学试卷(解析版) 题型:选择题
A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如下图所示。A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素。下列说法错误的是
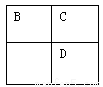
A. 简单离子的半径大小关系:B>C>E
B. C元素的气态氢化物比D元素的气态氢化物稳定是氢键的缘故
C. 由A、B两种元素组成的离子化合物NH5中,阴、阳离子个数比为1:1
D. 由C、D、E三种元素组成的某种化合物,其水溶液能与盐酸反应产生沉淀
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高一下期末化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值。下列说法正确的是
A.1.6 g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA
B.氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA
C.标准状况下,11.2 L苯中含有分子的数目为0.5NA,
D.在过氧化钠与水的反应中,每生成0.1 mol氧气,转移电子的数目为0.4NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期末化学试卷(解析版) 题型:选择题
a、b、c、d四种元素在周期表中的位置如下图,则下列说法正确的是

A. 若b的最高价氧化物对应水化物为H2bO4,则a的氢化物的化学式为aH3
B. 若a的核电荷数为z,则b的核电荷数一定为z+8
C. 最高价氧化物对应水化物的碱性强弱:b>c
D. a与b之间容易形成离子化合物
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期末化学试卷(解析版) 题型:选择题
下列有关钠和镁的说法中,不正确的是
A.金属镁燃烧后会发出耀眼的白光,因此常用来制造信号弹和焰火
B.金属钠在高温下能将TaCl4中的钛置换出来
C.金属镁着火,可用二氧化碳灭火
D.电解熔融NaCl可以得到金属钠
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二下期末化学试卷(解析版) 题型:简答题
【加试题】污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某研究小组利用软锰矿(主要成分为MnO2,另含少量铁,铝,铜,镍等金属化合物)作脱硫剂,通过如下简化流程,既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略)。
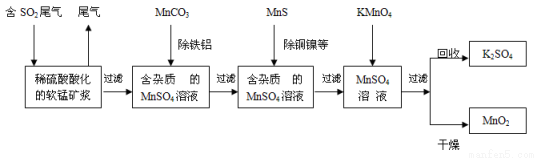
请回答下列问题:
(1)上述流程脱硫实现了 (选填下列字母编号)。
A.废弃物的综合利用 B.白色污染的减少 C.酸雨的减少
(2)用MnCO3能除去溶液中Al3+和Fe3+,其原因是 。
(3)已知:25℃、101kPa时,
Mn(s)+O2(g)=MnO2(s) ??ΔH = -520kJ/mol
S(s)+O2(g)=SO2(g) ?ΔH = -297kJ/mol
Mn(s)+S(s)+2O2(g)=MnSO4(s) ?ΔH = -1065kJ/mol
SO2与MnO2反应生成无水MnSO4的热化学方程式是 。
(4)MnO2可作超级电容材料。用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式是 。
(5)假设脱除的SO2只与软锰矿浆中MnO2反应。按照图示流程,将5 m3(标准状况)含SO2的体积分数为3 %的尾气通入矿浆,若SO2的脱除率为89.6%,最终每得到MnO2的质量1 kg,则除去铁、铝、铜、镍等杂质时,所引入的锰元素相当于MnO2 kg。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆哈密二中高二6月月考化学试卷(解析版) 题型:选择题
下列有关除去杂质的方法中,不正确的是(括号中的物质为杂质) ( )
A.苯(苯酚):加浓溴水,过滤
B.淀粉溶液(NaCl):半透膜,渗析
C.溴乙烷(乙醇):加蒸馏水,分液
D.乙酸乙酯(乙醇):加饱和碳酸钠溶液,分液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com