
| A. | 锡青铜的熔点比纯铜高 | |
| B. | 在自然环境中,锡青铜中的锡可对铜起保护作用 | |
| C. | 锡青铜文物在潮湿环境中的腐蚀比干燥环境中快 | |
| D. | 生成Cu2(OH)3Cl覆盖物是电化学腐蚀过程,但不是化学反应过程 |
分析 A、合金比成分金属有更优良的物理和化学性能,合金的硬度大,熔点低;
B、较活泼的金属能保护较不活泼的金属;
C、构成原电池能加快金属的腐蚀;
D、青铜是铜锡合金,在潮湿的环境下形成原电池.
解答 解:A、合金比成分金属有更优良的物理和化学性能,锡青铜属于合金根据合金的特性,熔点比任何一种纯金属的低,故A错误;
B、由于锡比铜活泼,故在发生电化学腐蚀时,锡失电子保护铜,故B正确;
C、潮湿的环境下,合金能构成原电池,将会加快金属的腐蚀速率,故C正确;
D、青铜是铜锡合金,在潮湿的环境下形成原电池,锡做负极,铜做正极,故生成Cu2(OH)3Cl不但是化学反应的过程,更是电化学腐蚀的过程,故D错误.
故选AD.
点评 本题考查合金的性质及影响金属的腐蚀速率的因素,注意原电池反应加快化学反应速率,题目难度中等.


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 34gH2O2中含有的阴离子数为1NA | |
| B. | 4.6g乙醇中含有的C-H键的个数为0.6NA | |
| C. | 标准状况下,VL水含有的氧原子个数约为$\frac{V}{22.4}$ | |
| D. | 1molFe2+与足量的H2O2溶液反应,转移NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 组分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
| 质量分数/% | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.16 |
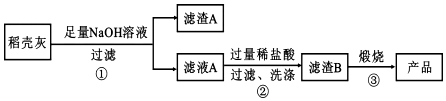
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向含有少量KSCN的FeI2溶液中滴加少量溴水,溶液出现血红色 | |
| B. | 用NH4HCO3固体以及其他固体药品能制得纯净的NH3 | |
| C. | 将SO2通入酸性KMnO4溶液中,溶液褪色,体现了SO2的漂白性 | |
| D. | 加热条件下,过量的Fe与浓硫酸反应只生成SO2一种气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1mol纯物质完全燃烧时所放出的热量,叫该物质的燃烧热 | |
| B. | 放热反应热化学方程式中△H就是该反应物的燃烧热 | |
| C. | 物质的燃烧热可利用仪器由实验测得 | |
| D. | 物质燃烧必然伴随发光发热现象且肯定是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 第I栏 | 第II栏 | 第Ⅲ栏 |
| A | 往少量NaOH溶液中投入铝片 | 往过量NaOH溶液中 投入铝片 | 2Al+2OH-+2H2O═2AlO2-+3H2↑ |
| B | 往Fe2( SO4)3溶液 中滴入氢氧化钠溶液 | 往Fe2 (SO4)3溶液 中滴入氢氧化钡溶 液 | Fe3++3OH=Fe(OH)3↓ |
| C | NaHCO3溶液滴入Ca(OH)2 | NaHCO3溶液滴入NaOH溶液 | Ca2++OH-+HCO3-=CaCO3↓+H2O |
| D | 往NaOH泪液中通入过量CO2气体 | 往NaOH溶液中通入少量CO2气体 | CO2+OH-=HCO3- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com