
| A、氨水应密闭保存 |
| B、500℃左右比常温下更有利于合成氨 |
| C、生产硫酸的过程中使用过量空气煅烧硫铁矿可以提高原料的利用率 |
| D、用纯碱溶液洗涤油污时加热效果更好 |


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
| 浓硫酸 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
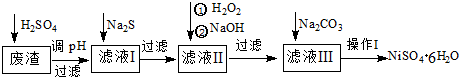
查看答案和解析>>
科目:高中化学 来源: 题型:
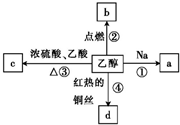 乙醇是生活中常见的有机物,能进行如图所示的多种反应,a、b、c、d都是含碳化合物.下列说法错误的是( )
乙醇是生活中常见的有机物,能进行如图所示的多种反应,a、b、c、d都是含碳化合物.下列说法错误的是( )| A、a的水溶液呈酸性 |
| B、反应②、④均为氧化反应 |
| C、c难溶于水 |
| D、可用金属钠区别乙醇和d |
查看答案和解析>>
科目:高中化学 来源: 题型:
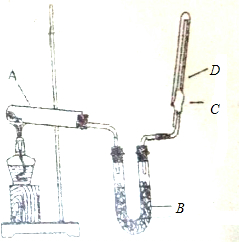 如图所示,实验室用NH4Cl和Ca(OH)2制取NH3.
如图所示,实验室用NH4Cl和Ca(OH)2制取NH3. 查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯与浓硝酸、浓硫酸共热并保持55-60℃反应生成硝基苯 |
| B、苯乙烯在合适条件下催化加氢可生成乙基环己烷 |
| C、乙烯与溴的四氯化碳溶液反应生成1,1-二溴乙烷 |
| D、CH3CH2Cl不属于烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10、2 | B、6、4 |
| C、8、2 | D、2、8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯中的甲苯(溴水分液) |
| B、乙醇中的水(新制CaO蒸馏) |
| C、乙醛中的乙酸(NaOH蒸馏) |
| D、乙酸乙酯中的乙酸(饱和Na2CO3溶液分液) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com